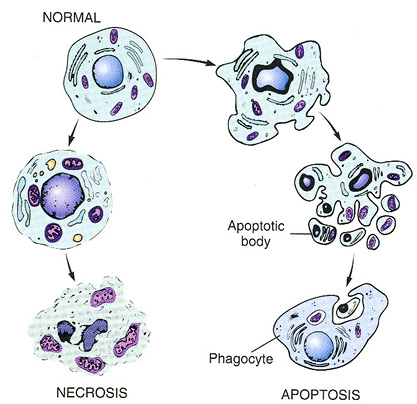
NEOPLAZİ
Beniğn yada maliğn her tümör iki ana komponentten oluşur.
1- Parankim: Çoğalan tümöral hücreler
2- Stroma: Bağ dokusu ve kan damarlarından oluşan destek doku
Belirgin kollajenöz stroma oluşumu dezmoplazi, yoğun stroma içeren tümörler skiröz olarak isimlendirilir. Karsinomlar sarkomlara kıyasla daha dezmoplazik, yani daha skiröz tümörlerdir. Örneğin: İnvaziv duktal meme karsinomu
İsimlendirme
Beniğn Tümörler:
Genellikle köken aldıkları hücre tipinin sonuna –oma eki alarak isimlendirilirler.
Yumuşak doku (mezenşimal) tümörlerinden fibroma, kondroma, osteoma gibi...
Epitelyal beniğn tümörler ise hücre tipi ve oluşturdukları yapıya göre isimlendirilir.
• Adenom : Glandüler yapılar oluşturan veya gland kökenli beniğn tümör.
• Papillom : Mikroskobik veya makroskobik parmaksı çıkıntılar yapan epitelyal beniğn tümör.
• Kistadenom – papiller kistadenom : Özellikle over ve apendikste epitel hücreleri ile döşeli, bazen lümene papiller çıkıntılar oluşturabilen kist oluşumu ile karakterli beniğn tümörler.
• Polip : Mide ve kolon gibi boşluklu organ-larda, mukozadan kabarık saplı veya sapsız (sesil) beniğn tümörler.
Maliğn tümörler (kanser):
• Mezenşimal kökenli maliğn tümörler, köken aldığı hücre tipinin sonuna sarkom eki alarak isimlendirilir. Liposarkom, Fibrosarkom, Kondrosarkom, Leiomyo-sarkom, Rabdomyosarkom vb.
• Epitelial kökenli maliğn tümörler ise köken aldığı hücre tipinin sonuna karsinom eki alırlar. Adenokarsinom, Skuamöz hücreli (yassı epitel hücreli) karsinom, transisyonel hücreli (değişici epitel hücreli) karsinom vb.
Beniğn gibi isimlendiren maliğn tümörler:
Seminoma, hepatoma, lenfoma, mezotelioma, kordoma, melanoma, hipernefroma (renal hücreli karsinom)
Mikst tümörler: Tek bir hücreden köken aldığı halde hem epitelial hemde mezenşimal diferansiasyon gösteren tümörlerdir.
- Pleomorfik adenom
- Fibroadenom
- Wilms tümörü
- Sinovial sarkom
- Maliğn mezotelioma
- Uterusun mikst müllerien (mezodermal) tümörleri (karsinosarkom)
-Memenin filloides tümörü
Örneğin: Fibroadenom ve filloides tümörleri memede lobül içi stroma hücresinden köken aldıkları halde, hem mezenşimal iğsi hücreli komponenti; hemde epitel hücreleri ile döşeli duktus ve yarık benzeri oluşumları bir ararda içerirler.
Teratom : Üç germ yaprağından köken alan germ hücre tümörüdür. Overde en sık görülen germ hücre tümörü olan matür kistik teratom (dermoid kist), kist lümeninde sebase materyal ve kıl, duvarda cilt, kas, yağ dokusu, barsak epiteli, diş yapıları gibi farklı germ yapraklarından köken alan elemanlar içerir. Genellikle baskın olan komponent ektodermdir.
Koristom : (Heterotopi) Normal bir doku örneğinin olması gerekenden farklı bir yerde bulunmasıdır. Mide mukozasında pankreas dokusu veya böbrek parankiminde adrenal dokusunun varlığı, Mekel divertikülünde mide mukozasının varlığı gibi..
Hamartom : Normalde belirli bir dokuyu oluşturan matür hücrelerin, gelişim defekti sonucu, aynı yerde düzensiz ve disorganize kitle oluşturmalarıdır. Klinikte kitle oluşturarak tümörle karışabilir. Mikroskobik olarak ayırımı kolaydır. Akciğerde en sık görülen beniğn lezyon hamartomdur.
Koristom ve hamartom tümör değil; tümöre benzer kitle yapan gelişimsel defektlerdir.
Beniğn – Maliğn Tümör Ayırımı
Diferansiasyon ve anaplazi, büyüme hızı, lokal invazyon ve metastaz ayırımda kullanılan kriterlerdir. En kesin maliğnite göstergesi metastazdır.
• Diferansiasyon : Tümörün köken aldığı hücreleri taklit edebilme yeteneğidir. İyi diferansiye tümörler düşük dereceli (grade’li), köken aldığı hücrenin özelliklerini taşıyan tümörlerdir ve mikroskobik incelemede kolay tanınırlar. Endokrin kökenli iyi diferansiye tümörler, hücrenin fonksiyonunuda taklit ederek hormon üretebilirler. Tümörün diferansiasyonu azaldıkça (az diferansiye, indiferansiye tümör) derecesi artar, prognozu bozulur ve tanısı zorlaşır.
• Anaplazi : Diferansiasyonun tamamen kaybıdır. Özellikleri:
- Pleomorfizm: Hücre ve hücre nüvesinde, boyut, şekil ve boyanma farklılığı
- Anormal nükleer görünüm: DNA içeriği artmış, hiperkromatik ve iri nüveler, belirgin nükleol varlığı
- Mitoz: Artmış tipik ve atipik (tripolar, quadripolar) mitozlar
- Polarite kaybı: Oryantasyon bozukluğu, polarite kaybı, anarşik, disorganize büyüme
- Diğerleri: Tümör dev hücreleri, tümör merkezinde iskemik nekroz
• Displazi: Bazal membranı aşmayan, intraepitelial gelişen, hücrelerde üniformite kaybı ve yapısal düzenlemede bozulma…Displastik değişiklikler belirgin olup, epitelin tüm kalınlığını içine alıyorsa: karsinoma in situ.. Hafif ve orta dereceli displazilerde, etken ortadan kaldırılırsa, epitel çoğu kez normale döner.
• Büyüme Hızı: Maliğn tümörler beniğn tümörlere göre daha hızlı büyümekle birlikte istisnalar olabilir. Örneğin hamilelikte östrojen artışına bağlı olarak leiomyom hızla büyüyebilir.
• Lokal İnvazyon: Metastazdan sonra malğnite tanısında ikinci önemli kriterdir. Beniğn tümörlerin çoğu kapsüllü olup çevre dokudan kolay ayrılırlar. (Kapiller hemanjiom ve pleomorfik adenom, beniğn oldukları halde halde invazivyon yapabilirler.) Maliğn tümörlerde ise çevre dokuya invazyon belirgindir ve operasyonda bir miktar normal çevre doku ile birlikte çıkarılmalıdır (radikal cerrahi).
• Metastaz : En kesin maliğnite kriteri olup primer tümörle devamlılığı olmayan tümör implantlarıdır. (Glial tümörler ve bazal hücreli karsinom maliğn olduğu halde uzak metastazları çok nadirdir.) Metastaz üç şekilde gerçekleşebilir.
1. Vücut boşlukları ve yüzeylerine direkt yayılım: En sık periton, daha nadiren plevra, perikard, subaraknoid bölge ve eklem boşluklarına olur. Peritonda over ve GİS tümörleri, plevrada akciğer ve meme karsinomları en sık rastlanan metastazlardır. Ayrıca lösemi ve lenfomada serozal yüzeylere yayılabilir. Medulloblastom ve ependimom subaraknoid yayılım gösterebilir.
2. Lenfatik yayılım: Daha çok karsinomların yayılım biçimidir. Lenf düğümü tutulumu genellikle drenaj yolunu izler. Zamanla karsinomlarda hematojen yayılım gösterebilir. Sarkom olduğu halde lenf nodu metastazı yapan tümörlere örnek olarak Kaposi sarkomu verilebilir.
Sentinel lenf nodu: Tümörün drene olduğu lenfatik bölgede, drenajı alan ilk lenf nodudur. Tümörün içine mavi boya yada radyoaktik madde verilerek, ilk drene olduğu lenf nodu bulunur. Meme karsinomunda, sentinel lenf nodu negatif ise, aksiler küretaja gerek kalmaz. Ayrıca melanom, kolon kanseri ve diğer tümörlerde de uygulanabilir.
3. Hematojen yayılım: Sarkomlar için tipik olmakla birlikte karsinomlarda da görülebilir. Yayılım genellikle ince duvarlı venler aracılığı ile olur. Arteriel yayılımın olabilmesi için venöz sistemle akciğere gelen tümörün akciğer engelini aşması veya primer odağın akciğerde olması gerekir. Venöz yayılım ön planda olduğundan vücutta en sık metastaza uğrayan organ akciğer, ikinci olarak karaciğerdir. Ayrıca adrenal gland, kemik ve beyinde sık metastaza uğrayan bölgelerdir. Karsinom olduğu halde hematojen yayılımın sık görüldüğü tümörler: Tiroid karsinomları (özellikle foliküler karsinom), prostat karsinomu, renal hücreli karsinom ve hepatoselüler karsinom
Beniğn-Maliğn Tümör Ayırımı
| Özellikleri |
Beniğn |
Maliğn |
| Diferansiasyon/anaplazi |
İyi diferansiye, köken aldığı dokuya benzer |
Diferansiasyon kaybı; anaplazi, yapısal atipi |
| Büyüme hızı |
Genellikle yavaş, büyüme durabilir, hatta gerileyebilir; mitotik figürler nadir ve tipik |
Yavaş yada hızlı olabilir; mitotik figürler sık ve atipik |
| Lokal invazyon |
Genellikle belirgin sınırlı; invazyon yok |
Lokal invaziv, çevre dokuları infiltre eder; bazen sınırlı görülür |
| Metastaz |
Yok |
Genellikle var; primer ne kadar büyük ve az diferansiye ise, metastaz o kadar sıktır |
Leiomoyom-Leiomyosarkom ayırımı
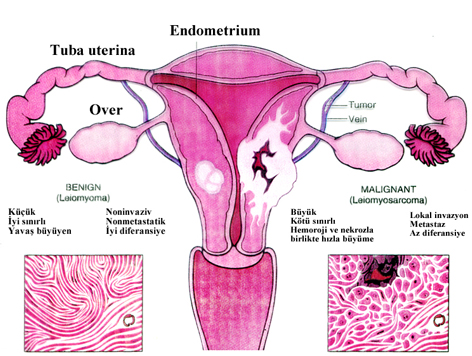
Epidemiyoloji
Kanser Sıklığı
Organ tümörleri içerisinde, erkekde en sık görülen tümörler prostat, akciğer ve kolorektal karsinomlardır. Kadında meme, akciğer, kolon ve rektum karsinomları sıktır. Akciğer karsinomu, her iki cinste, en sık ölüme yol açan tümördür.
Coğrafi ve Çevresel Faktörler
Japonya’da mide karsinomu; ABD ve Belçika’ da akciğer karsinomu sıktır. Yeni Zelanda’ da maliğn melanom; İzlanda’ya göre 6 kat fazladır.
Kişisel alışkanlıklar, çalışma ortamında maruz kalınan etkenler, besin maddeleri gibi pek çok çevresel etken kansere yol açabilir. Obesite risk faktörüdür.
Alkol : Orofarinks, larinks, özefagus, karaciğer kanserleri
Sigara : Ağız, farinks, özefagus, mide, pankreas, mesane, böbrek, serviks ve en önemlisi akciğer kanserleri
Alkol ve Sigara : Üst solunum – sindirim sistemi kanserleri riskini, birlikte kullanılınca, tek başına etkilerinden daha fazla arttırırlar.
Çalışma Ortamındaki Karsinojenler
| Etken |
Kanser tipi |
Kullanım alanı |
| Arsenik |
Akciğer, cilt, hemanjiosarkom |
Metal eritme ürünü, elektrikli aletler, ilaçlar, herbisid ve fungusidler |
| Asbest |
Akciğer, mezotelioma, GİS (özefagus, mide, kalın barsak) |
Ateşe dayanıklı kumaşlar, döşeme ve duvar kağıtları, eskiden gemi yapımı |
| Benzen |
Lösemi, Hodgkin lenfoma |
Lamba yağları, baskı, boya, kuru temizleme, yapıştırıcı, deterjanlar |
| Berilyum |
Akciğer |
Yakıt ve uzay araçları, nükleer reaktörler |
| Kadmiyum |
Prostat |
Sarı pigment, fosfor, piller, metal kaplama |
| Krom |
Akciğer |
Metaller, boyalar, pigment ve koruyucular |
| Etilen oksid |
Lösemi |
Meyve ve kuruyemişlerin olgunlaştırılması, roketin fırlatılması, kimyasal sentez, gıda ve tekstilde ilaçlama, sterilizanlar |
| Nikel |
Burun, akciğer |
Nikel kaplama, seramik ve pil ürünleri |
| Radon |
Akciğer |
Uranyum içeren minerallerin çürümesi, madenler |
| Vinil klorid |
Anjiosarkom, karaciğer |
Dondurucu, plastikler için yapıştırıcı; eskiden aerosollerde bulunurdu, |
Yaş
Kanserlerin çoğu 55 yaş üzerinde görülür. 60-79 yaş arasında, kansere bağlı ölümlerde pik oluşur. 15 yaş altı çocuklarda kanserden ölüm oranı %10 olup, ABD’de kazalardan sonra ikinci ölüm nedenidir. Akut lösemi ve SSS tümörleri, bu ölümlerin %60’ını oluşturur.
Genetik Predispozisyon
Kanserle ilişkili sendromlar üç gruba ayrılabilir.
- Otozomal dominant geçiş gösteren kanser sendromları: Tümör süpresör (baskılayıcı) gen mutasyonları ile oluşurlar.
- Otozomal resesif geçiş gösteren herediter preneoplastik sendromlar: DNA tamir defektleri bu grupta yer alır.
- X’e bağlı resesif geçen immün yetmezlik sendromları: Herediter ve edinsel immün yetmezliklerde lenfoma ve lösemi riski artar
OD herediter kanser sendromları
• Familyal retinoblastom: Genellikle bilateral, osteojenik sarkom gibi ikincil tümörler
• Familyal adenomatöz polipozis koli: Sayısız polipöz adenomlar, profilaktik kolektomi yapılmazsa 50 yaş civarında %100 kanser gelişimi
• MEN tip I: Pituiter, paratiroid, pankreas ada hücreleri adenomları
• MEN tip II: Tiroid meduller karsinomu, feokromasitoma, paratiroid tümörleri
• MEN tip III: Tiroid meduller karsinomu, feokromasitoma, ganglionöromlar
• Nörofibromatozis tip I (von Recklinghausen hastalığı) : Multiple nöral tümörler (beyin ve optik sinir gliomları, feokromasitoma, nörofibrom, schwannom, menenjiom), café au lait lekeleri , pigmentli iris hamartomu (Lisch nodülleri), kemik defektleri ve maliğn periferik sinir kılıfı tümörü (MPSKT) riski
• Nörofibromatozis tip II: Bilateral akustik sinir tümörleri (schwannom, menenjiom) cilt tümörleri, café au lait lekeleri.. Lisch nodülleri görülmez. MPSKT riski var.
• Von Hippel-Lindau sendromu: Retina, serebellum, beyin sapı hemanjiomları, organ kistleri ve renal hücreli karsinom riski
• Wilms tümörü : Konjenital malformasyon ve böbrekte Wilms tümörü
• Li Fraumeni Sendromu: Meme, kolon kanserleri, sarkomlar gibi çok sayıda tümörler
• Herediter nonpolipoid kolon kanser (HNPCC): DNA tamir defekti…En sık görülen kanser predispozisyon sendromudur. Kolon, ince barsak, endometrium ve over tümörleri görülebilir.
OR herediter preneoplazik durumlar
• Kseroderma pigmentozum: Ciltte bazal hücreli ve skuamöz hücreli karsinom, melanom
• Bloom sendromu: Akut lösemi ve değişik karsinomlar
• Fankoni anemisi: Akut lösemi, skuamöz hücreli karsinom ve karaciğer kanser
• Ataksi-telenjiektazi: Akut lösemi, lenfoma, meme kanseri
X’e bağlı immün yetmezlikler
• X’e bağlı agamaglobulinemi: Lenfoma ve lösemi
• Wiskott-Aldrich sendromu: Akut lösemi, lenfoma
• X’e bağlı lenfoproliferatif sendrom: EBV’e anormal yanıt ve buna bağlı B hücreli immünoblastik lenfoma
Edinsel preneoplastik durumlar:
Rejeneratif, hiperplazik, metaplazik ve displazik durumlar tümöre yatkınlık oluşturursa da tümör riski oldukça düşüktür. Kronik atrofik gastrit, ciltte solar keratoz, ülseratif kolit, oral kavite – vulva – vajen ve penisde lökoplaki ve eritroplaki, villöz adenom, endometrial hiperplazi, skuamöz metaplazi, siroz gibi durumlar örnek verilebilir.
Ülseratif kolit, Crohn hastalığı, Helikobakter pylori gastriti, viral hepatit ve kronik pankratit gibi kronik inflamatuar olaylarda kanser riski artar. Bunun nedeni tam olarak bilinmese de, sitokinlerin trasforme hücrelerin çoğalmasını uyardığı düşünülmektedir. İnflamasyonda oluşan serbest radikaller mutajenik olabilir. Kolon kanseri gibi bazı tümörlerde COX-2 artışı belirlenmiş olup tedavide COX-2 inhibitörlerinin rolü araştırılmaktadır.
Kalıtsal Kanser Predispozisyonu
Otozomal dominant
| Gen |
Predispozisyon |
| RB |
Retinoblastom |
| p53 |
Li-fraumeni sendromu |
| p16INK4A |
Melanom |
| APC |
FAP/kolon kanser |
| NF1, NF2 |
Nörofibromatozis 1 ve 2 |
| BRCA1, BRCA2 |
Meme ve over tümörleri |
| MEN1, RET |
MEN 1 ve 2 |
| MSH2, MLH1, MSH6 |
Herediter nonpolipozis kolon kanser |
| PATCH |
Nevoid bazal hücreli karsinom |
| Otozomal Resesif |
|
| Kseroderma pigmentozum |
|
| Ataksi telenjiektazi |
|
| Bloom sendromu |
|
| Fankoni anemisi |
|
Kanserin Oluşumu
• Kalıtsal, çevresel etkenlerle ve spontan olarak oluşabilen genetik hasar (mutasyon) kanserin temelinde yatan nedendir.
• Genetik hasara uğrayan tek bir öncü hücre, çoğalarak tümörü oluşturur (monoklonal)
• Dört grup normal düzenleyici gende oluşan mutasyon kanser gelişiminde önemlidir: Çoğalmaya yol açan protoonkogenler; çoğalmayı durduran tümör süpresör genler; apoptoz genleri ve DNA tamir genleri…
• Genotipik ve fenotipik olarak, karsinogenez çok basamaklı bir süreçtir. Büyüyen tümörün lokal invazyon ve metastaz yapması, fenotipik olarak tümör progresyonudur. Moleküler düzeyde, tümörün progresyonu genetik lezyonların birikimi ile oluşur.
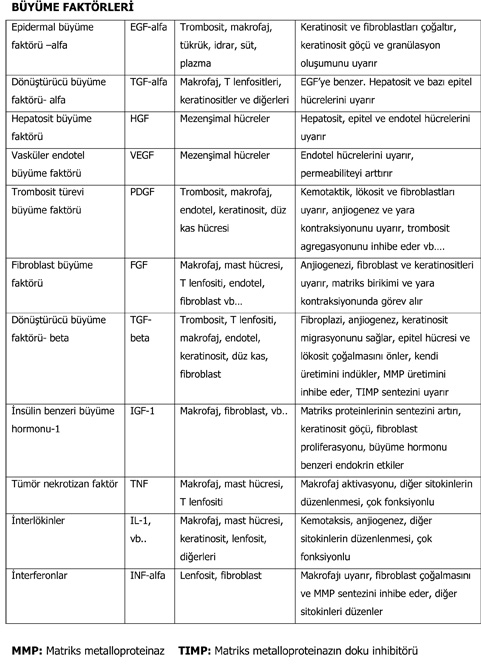
Hücre çoğalmasını sağlayan büyüme faktörleri, bunlara ait reseptörler, hücrede sinyal taşıyan proteinler ve transkripsiyon faktörlerini kodlayan genlere protoonkogen denir. Bunların mutasyonu ile ürünleri ve dolayısı ile hücre proliferasyonu artar. Hücre çoğalmasını ve siklusunu kontrol altında tutan tümör süpresör genlerin mutasyonu ise delesyondur. Görevlerini yapamazlar ve hücre proliferasyonu kontrolden çıkar.
Protoonkogen mutasyonu (onkogen) ve ilişkili olduğu tümörler
|
Kategori
|
Protoonkogen
|
Aktivasyon şekli
|
Tümör
|
|
Büyüme faktörleri
|
|
|
|
|
PDGF
|
SIS
|
Overekspresyon
|
Astrositom
Osteosarkom
|
|
FGF
|
HST-1
|
Overekspresyon
|
Mide, mesane, meme karsinomları, melanom
|
| |
INT-1
|
Amplifikasyon
|
|
|
TGF-alfa
|
TGF-alfa
|
Overekspresyon
|
Astrositom,hepatoselüler karsinom
|
|
HGF
|
HGF
|
Overekspresyon
|
Tiroid karsinomu
|
|
Büyüme faktör reseptörleri
|
|
|
|
|
EGF-resptör ailesi
|
ERB-B1
ERB-B2 (HER/2 neu)
|
Overekspresyon
Amplifikasyon
|
Akciğerde skuamöz karsinom, gliom
Meme, over karsinomu
|
|
CSF-1 reseptörü
|
FMS
|
Nokta mutasyonu
|
Lösemi
|
|
Nörotropik faktör reseptörü
|
RET
|
Nokta mutasyonu
|
MEN 2AveB, ailesel medüller tiroid karsinomu
|
|
PDGF reseptörü
|
PDGF-R
|
overekspresyon
|
Gliomlar
|
|
Kök hücre faktör reseptörü
|
KIT
|
Nokta mutasyonu
|
Gastrointestinal stromal tümörler ve diğer yumuşak doku tümörleri
|
|
Sinyal taşıyıcı proteinler
|
|
|
|
|
GTP-bağlama
|
K-RAS
H-RAS
N-RAS
|
Nokta mutasyonu
Nokta mutasyonu
Nokta mutasyonu
|
Kolon, akciğer, pankreas tümörleri
Mesane ve böbrek tm
Melanom, hematolojik tümörler
|
|
Nonreseptör tirozin kinaz
|
ABL
|
Translokasyon
|
KML, ALL
|
|
RAS sinyal iletimi
|
BRAF
|
Nokta mutasyonu
|
Melanom
|
|
WNT sinyal iletimi
|
Beta-katenin
|
Nokta mutasyonu Overekspresyon
|
Hepatoblastom, hepatoselüler karsinom
|
|
Nükleer düzenleyici proteinler
|
|
|
|
|
Transkripsiyon aktivatörleri
|
C-MYC
N-MYC
L-MYC
|
Translokasyon
Amplifikasyon
Amplifikasyon
|
Burkitt lenfoma
Nöroblastom, akciğer küçük hücreli karsinomu
Akciğer küçük hücreli karsinomu
|
|
Hücre siklus düzenleyicileri
|
|
|
|
|
Siklinler
|
CYCLIN D
CYCLIN E
|
Translokasyon
Amplifikasyon
Overekspresyon
|
Mantle zon lenfoma
Meme ve özefagus tm
Meme kanseri
|
|
Sikline bağlı kinazlar
|
CDK4
|
Amplifikasyon yada nokta mutasyonu
|
Glioblastom, melanom, sarkom
|
Kromozomal translokasyonlar, onkogenleri aktive ederler. Lösemi ve lenfomaların gelişimindeki temel mekanizma budur.
Onkogen Translokasyonu
| Maliğnite |
Translokasyon |
Etkilenen genler |
| Kronik myeloid lösemi |
(9;22) |
Abl(9), bcr (22) |
| AML ve ALL |
(4;11) |
AF4 (4), MLL (11) |
| Burkitt lenfoma |
(8;14) |
c-myc (8), IgH (14) |
| Mantle hücreli lenfoma |
-11,14 |
Cyclin D (11), IgH (14) |
| Foliküler lenfoma |
(14;18) |
IgH (14), bcl-2 (18) |
| T hücreli ALL |
(8;14) |
c-myc (8), TCR-alfa (14) |
| Ewing sarkom |
(11;22) |
FI-1 (11), EWS (22) |
Onkogenler ve Tedavi
• ERB-B2 (HER2 neu) mutasyonu, yalnızca tümör hücrelerinde olduğundan, buna yönelik antikorlar (transtuzumab) tedavide kullanılmaktadır. Buna hedeflenmiş tedavi denir.
• Diğer başarılı bir tedavi yöntemi ise, gastrointestinal stromal tümörlerde, c-KIT’in, reseptör tirozin kinaz aktivitesinin, imatinib ile bloke edilmesidir.
• KML ve bazı ALL olgularında, tirozin kinaz aktivitesi içeren protoonkogen c-ABL, 9. kromozomdaki normal yerinden koparak 22. kromozoma geçer ve BCR geni ile birleşir. Bu füzyon ile tirozin kinaz aktivitesi artar. İmatinib mezilat, BCR-ABL tirozin kinazı hedefleyerek tedavi sağlar. Toksisitesi düşüktür.
Tümör süpresör genler ve ilişkili oldukları tümörler
| Subselüler lokalizasyon |
Gen |
Fonksiyon |
Somatik mutasyonlu tümörler |
Kalıtsal mutasyonlu tümörler |
| Hücre yüzeyi |
TGF-beta reseptörü
E-cadherin
|
Büyüme inhibisyonu
Adezyon
|
Kolon karsinomu
Mide karsinomu
|
Bilinmiyor
Ailesel mide ca.
|
| Plazma membran iç yüzeyi |
NF-1 |
RAS sinyali ve p21 inhibisyonu |
Nöroblastom |
Nörofibromatozis 1 ve sarkomlar |
| Hücre iskeleti |
NF-2 |
İskelet stabilitesi |
Schwannom ve menenjiomlar |
Nörofibromatozis 2, akustik schwannom ve menenjiomlar |
| Sitozol |
APC/beta katenin |
Sinyal iletimi inhibisyonu |
Mide, kolon, pankreas ca. |
FAP/kolon ca. |
| PTEN |
PI-3 kinaz sinyal iletimi |
Endometrium ve prostat ca |
Bilinmiyor |
| SMAD2 ve SMAD4 |
TGF-beta sinyal iletimi |
Kolon, pankreas tm |
Bilinmiyor |
| Nüve |
RB |
Hücre siklus düzenleyicisi |
Retinoblastom, osteosarkom, meme, akciğer, kolon ca |
Retinoblastom, osteosarkom |
| P53 |
Hücre siklus arresti ve apoptoz |
Çoğu tümörler |
Li-Fraumeni sendromu, multiple karsinom ve sarkomlar |
| WT-1 |
Nükleer transkripsiyon |
Wilms tümörü |
Wilms tümörü |
| P16 (INK4a) |
Siklin bağımlı kinaz inhibisyonu |
Pankreas, meme, özefagus karsinomları |
Maliğn melanom |
| BRCA-1 ve BRCA-2 |
DNA tamiri |
Bilinmiyor |
Kadın meme ve over karsinomu; erkek meme karsinomu |
| KLF6 |
Transkripsiyon faktörü |
Prostat |
Bilinmiyor |
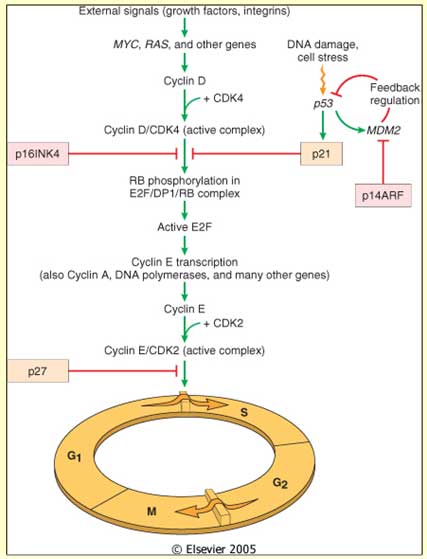
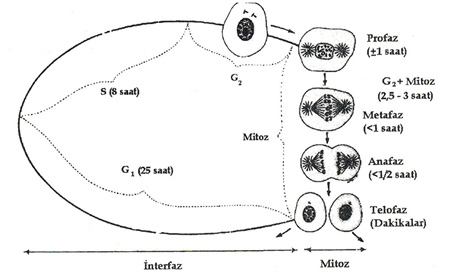
Hücreler G1, S, G2 ve M (mitoz) aşamalarını içeren hücre siklusuna girerek çoğalırlar. Bu siklusu başlatan myc, ras gibi onkogenlerin siklin ve siklin bağımlı kinazları uyarması ile oluşur. Bunlar hücre proliferasyonunu arttırırlar. Tümör baskılayıcı genler olan p53, p21, p14, p16, p27 ve Rb genleri ise gerektiği zaman devreye girerek hücre proliferasyonunu durdururlar. Böylece hücre çoğalması kontrol altında tutulur. Hücreler S fazına geçtikten sonra, bağımsız olarak çoğalmayı sürdürürler. Bu nedenle tümör baskılayıcı genlerin en önemli etki bölgesi G1 den S fazına geçiştir. Rb gen ürünü olan Rb proteini nükleer bir fosfoproteindir. Hipofosforilize olduğunda aktiftir ve hücre siklusunu G1-S fazı geçişinde durdurur. Fosforilize olduğunda inaktiftir ve hücre siklusu ilerler, hücreler çoğalmaya devam eder.
Hücre siklusunu düzenleyen protoonkogen ve tümör süpresör genlerde oluşan mutasyonlar sonucunda hücre çoğalması kontrolden çıkar ve maliğn tümör gelişme riski artar.
Apoptoz Genleri
• BCL-2 mutasyonu ile foliküler lenfoma gelişir. Foliküler lenfomaların %80’inde t(14;18) translokasyonu ile, 18. kromozomda yerleşen BCL-2, 14. kromozomdaki immünglobülin ağır zincir bölgesine geçer ve overeksprese olur. Apoptoz engellenir. B lenfositleri birikir ve yavaş çoğalan foliküler lenfomalar oluşur.
• MYC mutasyonu hücre çoğalmasını arttırarak, BCL-2 hücre ölümünü azaltarak tümör gelişiminde işbirliği yapabilirler.
• P53 mutasyonu varsa, BAX geni uyarılamaz ve apoptoz engellenir. Tümör riski artar. ¬
DNA tamir defektleri
• Herediter Nonpolipozis kanser sendromu: Çekum ve proksimal kolonda yerleşen tümörler ile karakterli, OD geçen bir kanser sendromudur. DNA eşleşme hataları oluşur. Örneğin, A ve T yerine, G ile T birleşir. Yanlış eşleşme tamir genlerinde defekt vardır. Protoonkogen ve tümör süpresör genlerde hatalı çiftlerin birikimi ile tümör riski artar. Endometrium ve over kanseride görülebilir.
• Kseroderma pigmentozum: Güneş ışınlerındaki UV etkisi ile cilt tümörleri gelişir. Primidin rezidülerinde çapraz bağlanma sonucunda DNA replikasyonu bozulur. Nükleotid eksizyon tamirinde defekt olduğu için DNA hasarı giderilemez.
• Diğerleri: Ataksi telenjiektazi ve Bloom sendromunda ionize radyasyona; Fankoni anemisinde ise DNA’yı çapraz bağlayan etkenlere karşı aşırı duyarlılık vardır. Ataksi telenjiektazi’de Purkinje hücrelerinin ilerleyici kaybı ile serebellar ataksi, defektif lenfosit proliferasyon ve matürasyonu ile immün yetmezlik, lenfoid maliğniteler, ionize radyasyona akut duyarlılık gelişir. ATM gen mutasyonu vardır. ATM, DNA hasarı oluştuğunda p53’ü uyarır. ATM eksikse, bu oluşmaz ve DNA tamiri ya da apoptoz başlatılamaz.
• BRCA-1 ve BRCA-2 genleri: BRCA-1 gen mutasyonu ile meme, over kanserleri yanı sıra prostat ve kolon kanseri riskinde hafif artış olur. BRCA-2 gen mutasyonu ise over ve erkek meme kanseri yanı sıra, melanom ve pankratik tümör riskini arttırır. Ailesel meme karsinomlarının çoğunda, bu genlerin mutasyonu belirlenirse de, diğer genlerden farklı olarak, sporadik olgularda etkileri gösterilememiştir.
Tümörde Anjiogenez
Tümörler beslenebilmek ve metastaz yapabilmek için damar oluşumunu uyarır (anjiogenez). Anjiogenez olmadan, 1-2 mm’den fazla büyüyemezler. İki önemli anjiogenik faktör; VEGF ve bFGF’ dir. Bunlar tümör hücreleri yada stromadaki makrofajlar tarafından üretilir. Anti-anjiogenik faktörler, trombospondin-1 (tümör hücreleri üretir), anjiostatin (plazminojen yıkım ürünü), endostatin ve tumstatindir (kollajen yıkım ürünleri). Endostanin ve tumstanin ile VEGF antikorları kanser tedavisinde denenmektedir.
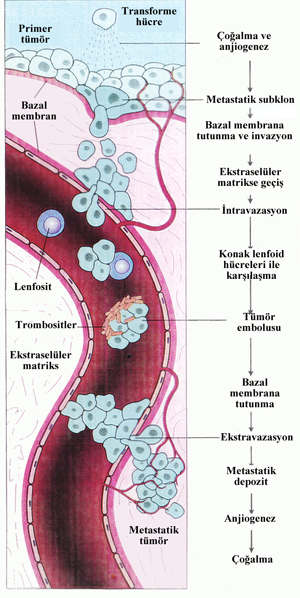
METASTAZ
Tümörün Yayılımı
Tümör büyümesi ve yayılımı dört aşamada gerçekleşir.
1-Transformasyon
2-Transforme hücrelerin çoğalması
3-Lokal invazyon
4-Metastaz
Çoğalan tümör hücreleri, bir taraftan yeni mutasyonlar geçirerek farklı subklonlar oluştururlar. Metastatik özellikler içeren subklon ne kadar erken gelişirse metastaz o kadar erken olur. Metastazın gelişmesinde bazı faktörlerin rolü vardır. Önce tümör hücreleri epitelial E-Cadherin gibi tutunma moleküllerini azaltarak ana kitleden koparlar. Daha sonra integrin reseptörleri ile laminin ve fibronektine tutunarak bağ dokusuna geçerler. Tümör hücreleri ve stroma hücrelerinden salgılanan proteazlar ile bazal membran ve bağ dokusu sindirilerek hücrelerin yolu açılır. Bunlar serin, sistein ve matriks metalloproteinaz (MMP)grubu proteazlardır. Sistein grubu proteazlardan katepsin D yüksekliğinin meme karsinomunda kötü prognoz bulgusu olduğu ileri sürülmektedir.
Damar endotelini aşarak dolaşıma giren tümör hücrelerine karşı ilk savaşan doğal öldürücü (NK) hücrelerdir. Trombositler ise tümör hücrelerinin yüzeyini örterek NK hücrelerinden korurlar Daha sonra T lenfositleri de devreye girerek tümöre karşı savaşır. Özellikle virüs etkisi ile oluşan tümörlerde sitotoksik T lenfositleri ön plandadır. Yerleşeceği bölgeye gelince endotel hücresine tutunan tümör hücreleri dışarı çıkarak integrin reseptörleri ve proteazların yardımı ile yerleşerek çoğalmaya devam eder. Tümör hücrelerindeki adezyon moleküllerinden CD44 (normalde T lenfositlerinde bulunur), tümör hücrelerinin ekstravazasyon ve yerleşmesinde rol oynar.
Hangi tümörün nereye metastaz yapacağı önceden kesin olarak belirlenemese de prostat karsinomu ön planda vertebraya; akciğer karsinomu adrenal gland, kemik ve beyine; nöroblastom karaciğer ve kemiğe metastaz yapar. Tümör hücreleri, hedef organ endoteline tutunabilen adezyon molekülleri içerebilir. Hedef organ, tümör hücreleri için kemotaktik olan, insülin benzeri büyüme faktörü I ve II üretebilir. Antiproteaz içeren çizgili kas dokusuna tümör hücrelerinin yerleşmesi zordur . Bu nedenle çizgili kasa metastaz nadirdir. Avasküler olan kornea ve kıkırdak gibi dokulara uzak metastaz oluşmaz.
Karsinojenik Ajanlar
Kimyasal karsinojenler
İnisiasyon ve promosyon olmak üzere iki basamakta etki ederler. İnisiasyonda mutasyon oluşur. Promotörlerin etkisi ile mutant hücrenin çoğalması sağlanır ve böylece transformasyon gerçekleşir. Promotörler tek başına mutajenik değildir. Önce inisiatörlerin mutasyon oluşturması gerekir. Kimyasal karsinojenler en sık RAS mutasyonuna yol açar. DNA tamir defektlerinde inisiasyon daha kolaydır ve oluşan mutasyon tamir edilemez.
İnisiatör ajanlar:
- Direkt etkililer : Beta propiolakton, Dimetil sülfat, Diepoksibütan, asetilleyici ve alkile edici antikanser ilaçlar. Kanser tedavisi sırasında lösemi, lenfoma ve diğer maliğniteler gelişebilir.
- İndirekt etkililer : p450 enzim sisteminde aktive edilirler. Metabolitleri karsinojeniktir. Fenobarbital p450 enzim sistemini indükleyerek indirekt etkili karsinojenlerin etkisini arttırır. Alkolde aynı şekilde etki edebildiğinden alkol ve sigaranın birlikte kullanılması riski tek başlarına olduklarından çok daha fazla arttırır.
• Polisiklik-heterosiklik aromatik hidrokarbonlar : Benzopiren gibi ürünler sigara dumanı, tütsülenmiş veya ateşe yakın pişirilmiş ızgara etlerde bulunurlar. Cilt, akciğer ve mesane kanseri ile sarkomlara yol açabilirler.
• Aromatik amin, amid, Azo boyaları: naftilamin , benzidin gibi ürünler karaciğerde metabolize olduğundan karaciğer ve mesane kanseri ile ilişkilidir.
• Doğal yolla oluşanlar: Aflatoksin B1, griseofulvin, safrol, sikazin vb. Aflatoksin Aspergillus flavus ‘un ürünü olup uygun koşullarda depolanmayan mısır, pirinç ve fındık gibi ürünlerde bulunur. Hepatoselüler karsinoma yol açar. HBV ile birlikte olduğunda, özellikle Çin gibi ülkelerde, risk çok artar.
• Nitrozamin ve amidler: Gıdalara koruyucu madde olarak katılan nitritler gastrointestinal sistemde dönüşüme uğrayarak özefagus ve mide kanserine yol açabilir.
• Aflatoksin, asbest, vinil klorid gibi meslek ortamında maruz kalınan kimyasal etkenlerde indirekt etkili karsinojenlerdir.
Promosyon : Forbol esterleri (TPA), hormonlar, fenoller, ilaçlar
Protein kinaz C aktivasyonu ile hücre çoğalmasını arttırırlar. İnisiasyon sonrası mutasyona uğrayan hücre çoğaldıkça maliğnite riski artar. Hormonlardan östrojen endometrial hiperplazi oluşturarak hücre çoğalmasını arttırır. DES kullanımı, benzer şekilde tümöre yol açabilir. Alkol ve safra tuzlarınında promotör etkisi olduğu ileri sürülmüştür.
Radyasyon karsinojenezi
• Ultraviole :UVB ışınları primidin dimerleri oluşturarak DNA mutasyonuna yol açar. Skuamöz (yassı epitel) hücreli ve bazal hücreli karsinom ile maliğn melanom riskini arttırır. İmmün yetmezlik varsa risk daha çok artar.
• Kseroderma pigmentozum, aşırı fotosensitivite, güneşe maruz kalan ciltte 2000 kat tümör riski artışı ve bazen nörolojik anomalilerle karakterli, OR geçişli bir DNA tamir defektidir.
• İonize radyasyon : En sık lösemi (KLL hariç) ve tiroid karsinomu (papiller) görülür. Daha az oranda meme, akciğer, tükrük bezi (mukoepidermoid karsinom) tümörleri oluşur. Cilt, gastrointestinal sistem ve kemik; radyasyona bağlı tümör gelişimine nispeten dirençlidir. Yine de, yeterli düzeyde radyasyona maruz kalan her hücre, kanser hücresine dönüşebilir. Karsinojenik etkisi dışında, iyonize radyasyon, akut dönemde, hızla çoğalan hücrelerde hasar ve ölüm oluşturur. Kemik iliği hücreleri, germ hücreleri, GİS epitel hücreleri hızla zedelenir. Periferik sinir, olgun kemik ve nöronlar nispeten dirençlidir.
Enfeksiyöz Karsinojenler
DNA virüsleri:
• HPV: Tip 16,18,31,33,35,51 serviks ve anogenital skuamöz hücreli karsinom, bazen ağız ve larinks karsinomu, Tip 6,11 (düşük risk) kondilom, Tip 1,2,4,7 skuamöz papillom (siğil). Maliğn tipleri direkt etkilidir. E6 proteini p53’e; E7 proteini Rb genine bağlanır ve inisiatör etki yapar. Sigara, mikrobial enfeksiyonlar, beslenme bozuklukları ve hormonal değişiklikler kofaaktör olarak rol oynar. İmmün yanıt da önemlidir.
• Epstein Barr virüsü : Burkitt lenfoma, B hücreli lenfomalar (öz. AİDS ve transplantasyon), bazı Hodgkin olguları, nazofaringeal karsinomlar (lenfoeepitelioma) ve immun yetmezlikte leiomyosarkom gelişimine yol açar. EBV, orofarinks ve CD21 molekülü aracılığı ile B lenfositlerini enfekte eder. Enfeksiyon latent olup lenfositi öldürmez ama immortalize edebilir. EBV, direkt karsinojenik değildir. Genetik ve çevresel faktörlerde etkilidir.
• HSV tip 8: Kaposi sarkomu, AIDS’li hastada effüzyon lenfoması (B hücreli) ve mulitiple myelomda suçlanmaktadır.
• Hepatit B virüsü: Hepatoselüler karsinom ile ilşkilidir. Uzak doğu ve Afrika’da endemiktir. Tayvan’ da HBV ile enfekte olanlarda tümör riski, olmayanlara göre 200 kat yüksektir. Tek başına direkt etkili değildir. Aflatoksin ile birlikte, direkt etki yapabilir. Virüsün HBx proteini, p53’ü etkileyerek hücre çoğalmasını arttırabilir.
RNA virüsleri
• HTLV-1 : CD4+T lenfositlerinin maliğn tümörü olan T hücreli lösemi/ lenfomayı oluşturur. Japonya ve Karayiplerde endemik; diğer bölgelerde sporadiktir. Cinsel ilişki, kan ürünleri ve emzirme ile enfekte T lenfositleri bulaşır. Enfekte olanların %3-5 kadarında, 40-60 yıl sonra tümör gelişir. Lösemi yanı sıra, tropikal spastik paraparezi denilen demyelinizan hastalık, uveit ve artrit gelişebilir.
• Hepatit C virüsü : Kronik karaciğer hasarı ve inflamasyonu izleyerek oluşan rejenerasyon, genetik instabilite ve tümör gelişimine yol açabilir.
Helikobakter Pylori
Kronik gastritli hastaların %90’ında H.pylori mevcuttur. Çoğunda klinik tablo oluşturmaz. %20-30 ülsere yol açar. Az olguda karsinom ve lenfoma oluşturabilir. CagA (sitotoksin ile ilişkili gen A) geni içeren grubu ile hastalık daha sıktır. Virulansla ilişkili VacA geni, apoptoza yol açar.
• Kronik gastrit, multifokal atrofi ve düşük asit sekresyonu, intestinal metaplazi ve displazi üzerinden, intestinal tipte gastrik karsinoma yol açar.
• H. Pylori, B hücrelerinin aktif proliferasyon göstererek t(11;18) translokasyonu gibi genetik anomaliler edindiği lenfoid infiltrasyonlara yol açar. Mukoza ile ilişkili lenfoid doku tümörleri olan MALT (marginal zon) lenfoma oluşur. H. Pylori tedavisi ile tümör gerileyebilir.
Klinik Bulgular
• Lokal ve hormonal etkiler: Hipofiz adenomu, beniğn olduğu halde, sağlam kalan hipofizide sıkıştırarak ağır endokrinopati yapabilir. Yada lümeni tıkayan bir tümör, barsakda obstrüksiyon oluşturabilir. Endokrin organ tümörlerinde, üretilen hormon artabilir. Tümörün oluşturduğu destrüktif büyüme ülserasyon, kanama ve sekonder enfeksiyonlar oluşturabilir.
• Kaşeksi: İlerleyici kilo kaybı, güçsüzlük, iştahsızlık ve anemi ile karakterlidir. En önemli etken tümör hücreleri ve makrofajlar tarafından üretilen TNF (kaşektin) dir. Ayrıca IL-1 ve INF-gama gibi sitokinler etkili olabilir.
• Paraneoplastik sendromlar: Tümörün lokal yada uzak yayılımı veya normalde o hücre tipi tarafından üretilemeyen hormon veya peptid benzeri maddelerin üretilmesi ile oluşan klinik tablolardır. En sık görülen endokrinopati Cushing sendromudur. En sık akciğer ve özellikle de küçük hücreli karsinom ile birlikte görülür. En sık görülen paraneoplastik sendrom ise hiperkalsemidir. Gri-siyah plaklar şeklinde hiperkeratotik lezyonlar ile karakterli Akantozis nigrikans, 40 yaş üzerinde görülürse, %50 maliğnite ile ilişkilidir. DİK, en sık akut promyelositik lösemi ve prostat karsinomu ile ilişkilidir.
Paraneoplastik Sendromlar:
|
Klinik sendrom
|
Kanser tipi
|
Mekanizma
|
|
Cushing’s sendromu
|
Akc.küçük hücreli ca.
Pankreatik ca
Neural tm.
|
ACTH veya benzer maddeler
|
|
Uygunsuz ADH salınımı
|
Akc. Küçük hücreli ca
İntrakranial neoplazmalar
|
ADH veya atrial natriüretik hormonlar
|
|
Hiperkalsemi
|
Akc. Yassı epitel hüc. ca
Meme ca
Renal ca
EriştinT.hüc.lösemi/lenfoma
Over ca
|
Parathormon ilişkili peptidler
TGF-a, TNFa, IL-1
|
|
Hipoglisemi
|
Fibrosarkom
Diğer mezenşimal tm.
Hepatosellüler ca
|
İnsülin veya benzer maddeler
|
|
Karsinoid send.
|
Bronşial adenom(karsinoid)
Pankreatik ca.
Gastrik ca.
|
Serotonin, bradikinin?
Histamin
|
|
Polisitemi
|
Renal ca
Serebellar hemanjiom
Hepatosellüler ca.
|
Eritropoetin
|
|
Sinir ve kas sendromları
|
|
Myastenya
Santral, periferal sinir sist. Boz.
|
Bronkojrnik ca, Timoma
Meme ca
|
İmmunolojik? Toksik?
|
|
Dermatolojik bozukluklar
|
|
Akantozis nigrikans
Dermatomyozit
|
Gastrik ca
Akc. ca
Uterin ca
Bronkojenik, meme ca
|
İmmunolojik ? EGF sekresyonu ?
|
|
Kemik, eklem, yumuşak doku değişiklikleri
|
|
Hipertrofik osteoratropati ve çomak parmak
|
Bronkojenik ca
|
Bilinmiyor
|
|
Vasküler-hematolojik değişiklikler
|
|
Venöz tromboz (tarusseau bulgusu)
Nonbakteriel trombotik
Endokardit
Anemi
|
Pankreas ca.
Bronkojenik ca.
Diğerleri
Yaygın kanserler
Timik tümörler
|
Tümör ürünleri (müsin)
Pıhtılaşmayı uyarır
Hiperkoagulabilite
Bilinmiyor
|
|
Diğerleri
|
|
Nefrotik sendrom
|
Melanom, Akc. Ve kolon ca
|
Tümör antijeni, immun kompleksler
|
• Evre : Kanserin yayılım düzeyidir. Primer lezyonun büyüklüğü, bölgesel lenf bezlerine yayılımı, uzak metastaz değerlendirilir. Metastaz yapan tümörlerde en önemli prognoz faktörü evredir.
• Derece (grade): Diferansiasyon düzeyi ve mitoz sayısının değerlendirilmesidir. GradeI-IV arası derecelendirme yapılır. Anaplazik tümörler grade IV’ dür. Evre kadar olmasa da, prognozda önemlidir.
Tanı:
• Histolojik – sitolojik yöntemler:
1- Sitolojik yaymalar: Pap smear, üriner sitoloji, meme başı akıntısı vb.
2- İğne aspirasyonu: Tiroid, meme, karaciğer lezyınları vb.
3- Biopsi yada eksizyon: İnsizyonel biopsi (tru-cut), total eksizyon yada radikal operasyon
• İmmunhistokimya:
1- İndiferansiye tümörlerde kategorizasyon: Sitokeratin pozitif ise karsinom; vimentin pozitif ise sarkom; demsin pozitif ise rabdomyosarkom gibi..
2- Lösemi ve lenfomaların kategorizasyonu: CD20 pozitif ise B hücreli; CD3 pozitif ise T hücreli gibi.
3- Metastatik tümörlerin kökeninin belirlenmesi: Metastaz yapan tümör hücrelerinde PSA pozitif ise, prostat karsinomu metastazıdır vb..
4- Prognostik ve terapötik önemi olan moleküllerin belirlenmesi: Meme karsinomunda östrogen ve progesteron reseptörlerinin varlığının belirlenmesi gibi..
• Moleküler tanı:
1- Lösemi ve lenfomalarda gen mutasyonlarını belirleyerek tanı koyma,
2- Tümör prognozunu belirlemek için genetik araştırma,
3- Minimal rezidüel hastalığın belirlenmesi,
4- Herediter kanser predispozisyonunun belirlenmesi,
5- DNA mikroarray analiz ile kanser hücrelerinin profilinin belirlenmesi
• Flow sitometri (akım sitometrisi):
1- Hücre yüzey antijenlerinin belirlenerek lösemi ve lenfomaların sınıflanması,
2- DNA içeriğinin araştırılması (ploidi)
• Tümör belirleyicileri
| Belirleyici (marker) |
Kanserin türü |
| Hormonlar |
|
| HCG |
Trofoblastik tm, nonseminomatöz testiküler tümörler |
| Kalsitonin |
Trioid meduller karsinomu |
| Kateşolamin ve metabolitleri |
Feokromasitoma ve benzeri tümörler |
| Ektopik hormonlar |
Paraneoplastik sendromlar |
| Onkofetal antijenler |
|
| Alfa - fetoprotein |
Karaciğer tümörleri, nonseminatöz testis germ hücreli tümörleri |
| Karsinoembriyojenik antijen |
Kolon, pankreas, akciğer, mide, meme ca. |
| İzoenzimler |
|
| Prostatik asid fosfataz |
Prostat karsinomu |
| Nöronspesifik enolaz |
Akciğer küçük hücreli karsinomu, nöroblastom |
| Spesifik proteinler |
|
| İmmunglobulinler |
Multiple myelom ve diğer gamapatiler |
| PSA |
Prostat karsinomu |
| Musinler ve diğer glikoproteinler |
|
| CA-125 |
Over karsinomu |
| CA-19-9 |
Kolon ve pankreas karsinomu |
| CA-15-3 |
Meme karsinomu |
| Yeni moleküler belirleyiciler |
|
| Gaita ve serumda p53, APC, RAS mutasyonları |
Kolon kanseri |
| Gaita ve serumda p53 ve RAS mutasyonları |
Pankreas karsinomu |
| Balgam ve serumda p53 ve RAS mutasyonları |
Akciğer kanseri |
| İdrarda p53 mutasyonu |
Mesane kanseri |
Read more















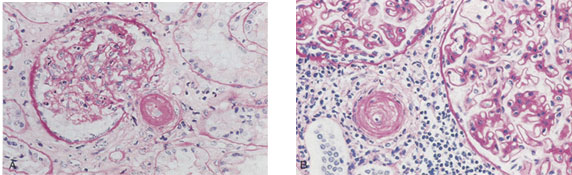
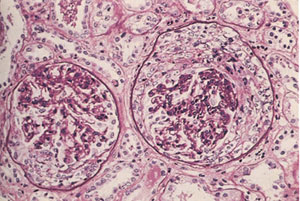
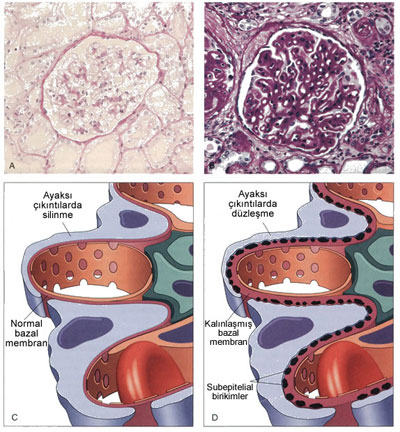 Membranöz Glomerülonefrit
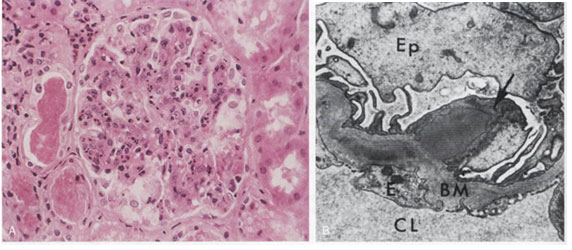
Membranöz Glomerülonefrit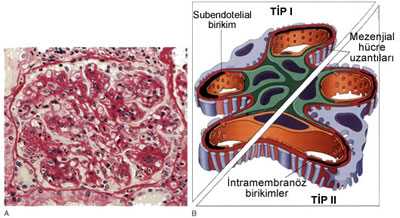



 Ekonomik olsun diye indirimli sitelerden (bravofly) aktarmalı bilet aldım. Alitalia ile Roma aktarmalı gittim. Roma da 4 saat ara vardı. 30 dakikada direkt Roma’ya giden Leonardo Ekspress (14 euro tek yön) ile şehre gidip gezme fırsatım oldu. Dönerken KLM ile Amsterdam aktarmalı döndüm. Süre kısaydı. Şehri gezemedim. Varış saatleri lokal saat ile. Roma ile 1 saat; Lİzbon ile 2 saat farkımız var. Örneğin saat 10’da Lizbon’a varış gözüküyorsa, bu Türkiye saati ile 12 oluyor. Hava alanından otobüs var ama taksi ile daha kolay. Bagaj başına ek ücret alınsa da, 10-13 euro civarında tutuyor. Taksiler gece ve tatil günlerinde az bir miktar ek alıyor. Şehir içinde metro, tramvay, tren ve otobüs hatları yoğun ve birbiri ile bağlantılı.
Ekonomik olsun diye indirimli sitelerden (bravofly) aktarmalı bilet aldım. Alitalia ile Roma aktarmalı gittim. Roma da 4 saat ara vardı. 30 dakikada direkt Roma’ya giden Leonardo Ekspress (14 euro tek yön) ile şehre gidip gezme fırsatım oldu. Dönerken KLM ile Amsterdam aktarmalı döndüm. Süre kısaydı. Şehri gezemedim. Varış saatleri lokal saat ile. Roma ile 1 saat; Lİzbon ile 2 saat farkımız var. Örneğin saat 10’da Lizbon’a varış gözüküyorsa, bu Türkiye saati ile 12 oluyor. Hava alanından otobüs var ama taksi ile daha kolay. Bagaj başına ek ücret alınsa da, 10-13 euro civarında tutuyor. Taksiler gece ve tatil günlerinde az bir miktar ek alıyor. Şehir içinde metro, tramvay, tren ve otobüs hatları yoğun ve birbiri ile bağlantılı. 3- YEME-İÇME: Portekiz mutfağı deniz ürünleri üzerine kurulu. Et yemekleri de var tabii ama ben de deniz ürünlerini tercih ettim. Genellikle yemeklerden önce aperatif olarak beyaz porto şarabını tercih ettim. Yanına yağ, peynir ve ekmek getiriyorlar (0,80-1 euro). Yemekle birlikte ev şarabını tercih ettim. Bacalhau denilen tuzlanmış morina balığı, soğan ve patates ile hazırlanan yemeği birkaç farklı türde yedim. Kremalı olanı da denedim (Rossio meydanı- Nicola ve Bairro alto- Das Gaveas) . Bana biraz yağlı ve tuzlu geldi. Ama gitmişken yememek olmaz. Denize girmek için gittiğim Cascais’de değişiklik olsun diye Hint lokantasına gittim. Tren istasyonunun karşı sokağında. Hint-İtalyan lokantaları genellikle birlikte oluyor. Dana şiş ve büryan pilavı yedim. Porsiyonları büyüktü, bitiremedim. Hard rock cafe, Rossio meydanında. İç dizaynı, müzikleri ve içkileri güzel. Üst katta yemek, alt katta içki servisi yapılıyor. İstanbul’a da şube açtık dediler. İstanbul’da gitmeye fırsatım olmayabilir dedim. Şaşırdılar ve güldüler. Gerçek büyük şehir hayatını bilmiyorlar tabii. Genellikle, bir kişilik yemek, şarap yada bira, üzerine kahve içildiğinde 25-30 euro civarında. Praça do comercio’ da Bira müzesinde atıştırmalıklarla birlikte, değişik biraları tattım. 15 eoro civarında tuttu. İstanbul’a kıyasladığınızda, yediğiniz yemekler de güzel olduğundan çok pahalı değil ama euro arttıkça bize daha pahalı gelecek tabii. Ben yine de önce Yunanistan, sonra da İspanya mutfağını tercih ederim. Endülüs’te, Tarifa’da yediğim balık ve midyenin lezzetini unutamıyorum.
3- YEME-İÇME: Portekiz mutfağı deniz ürünleri üzerine kurulu. Et yemekleri de var tabii ama ben de deniz ürünlerini tercih ettim. Genellikle yemeklerden önce aperatif olarak beyaz porto şarabını tercih ettim. Yanına yağ, peynir ve ekmek getiriyorlar (0,80-1 euro). Yemekle birlikte ev şarabını tercih ettim. Bacalhau denilen tuzlanmış morina balığı, soğan ve patates ile hazırlanan yemeği birkaç farklı türde yedim. Kremalı olanı da denedim (Rossio meydanı- Nicola ve Bairro alto- Das Gaveas) . Bana biraz yağlı ve tuzlu geldi. Ama gitmişken yememek olmaz. Denize girmek için gittiğim Cascais’de değişiklik olsun diye Hint lokantasına gittim. Tren istasyonunun karşı sokağında. Hint-İtalyan lokantaları genellikle birlikte oluyor. Dana şiş ve büryan pilavı yedim. Porsiyonları büyüktü, bitiremedim. Hard rock cafe, Rossio meydanında. İç dizaynı, müzikleri ve içkileri güzel. Üst katta yemek, alt katta içki servisi yapılıyor. İstanbul’a da şube açtık dediler. İstanbul’da gitmeye fırsatım olmayabilir dedim. Şaşırdılar ve güldüler. Gerçek büyük şehir hayatını bilmiyorlar tabii. Genellikle, bir kişilik yemek, şarap yada bira, üzerine kahve içildiğinde 25-30 euro civarında. Praça do comercio’ da Bira müzesinde atıştırmalıklarla birlikte, değişik biraları tattım. 15 eoro civarında tuttu. İstanbul’a kıyasladığınızda, yediğiniz yemekler de güzel olduğundan çok pahalı değil ama euro arttıkça bize daha pahalı gelecek tabii. Ben yine de önce Yunanistan, sonra da İspanya mutfağını tercih ederim. Endülüs’te, Tarifa’da yediğim balık ve midyenin lezzetini unutamıyorum.
 4- ÇEVRE GEZİLERİ: Önce metro, sonra da Cais do Sodre istasyonunundan trene binerek 30 dk içerisinde, okyanus kıyısındaki Cascais’e gidip okyanusta yüzebilirsiniz. Yol üzerinde Estoril var. İnip gezebilirsiniz. Ian Fleming, burada çok zaman geçirirmiş ve Casino Royale adlı James Bond filminin senaryosunu, buradaki Casino’dan esinlenerek yazmış. Ben direkt Cascais’e gittim. Trenden inince şöyle bir bakınıp deniz kenarına gittim. Plajda ücretli ve ücretsiz kısımlar var. Ben ücretli kısma geçtim. Şezlong ve şemsiye 14 euro ama kabin yada düzgün bir duş yok. Büyükçe bir tuvalet var. Orada giyinip soyunmak gerekiyor. Tek olduğundan önünde uzun kuyruk var. Hatta güneş çarpması nedeniyle, kuyrukta beklerken bayılan bir kıza müdahele etmem bile gerekti. Arkada yemek yenecek yada içki içilecek kafe-barlar var. Deniz oldukça soğuk, çok temiz gelmedi bana. Trenle dönerken, biraz daha ilerde daha güzel plajlar gördüm. Benim gibi hemen ilk gördüğünüze atlamayın. Rossio meydanına yakın olan tren garından ise Sintra’ya çok sık tren var. Benim vaktim kalmadığı için gidemedim. Kraliyet ailesinin yazlık şatosunun da bulunduğu, yeşillikler içinde tarihi bir bölgeymiş. Ayrıca Porto’ya gidenlerde çok övdüler. Artık bir dahaki sefere…
4- ÇEVRE GEZİLERİ: Önce metro, sonra da Cais do Sodre istasyonunundan trene binerek 30 dk içerisinde, okyanus kıyısındaki Cascais’e gidip okyanusta yüzebilirsiniz. Yol üzerinde Estoril var. İnip gezebilirsiniz. Ian Fleming, burada çok zaman geçirirmiş ve Casino Royale adlı James Bond filminin senaryosunu, buradaki Casino’dan esinlenerek yazmış. Ben direkt Cascais’e gittim. Trenden inince şöyle bir bakınıp deniz kenarına gittim. Plajda ücretli ve ücretsiz kısımlar var. Ben ücretli kısma geçtim. Şezlong ve şemsiye 14 euro ama kabin yada düzgün bir duş yok. Büyükçe bir tuvalet var. Orada giyinip soyunmak gerekiyor. Tek olduğundan önünde uzun kuyruk var. Hatta güneş çarpması nedeniyle, kuyrukta beklerken bayılan bir kıza müdahele etmem bile gerekti. Arkada yemek yenecek yada içki içilecek kafe-barlar var. Deniz oldukça soğuk, çok temiz gelmedi bana. Trenle dönerken, biraz daha ilerde daha güzel plajlar gördüm. Benim gibi hemen ilk gördüğünüze atlamayın. Rossio meydanına yakın olan tren garından ise Sintra’ya çok sık tren var. Benim vaktim kalmadığı için gidemedim. Kraliyet ailesinin yazlık şatosunun da bulunduğu, yeşillikler içinde tarihi bir bölgeymiş. Ayrıca Porto’ya gidenlerde çok övdüler. Artık bir dahaki sefere…