Hücrelerin normal fizyolojik ihtiyaçlarını karşılayarak hayatlarını sürdürmesi homeostaz olarak isimlendirilir. Hücrelerin zedeleyici bir etken yada ağır fizyolojik stresle karşılaştığında yeni koşullara uyum sağlamaya çalışmasına adaptasyon denir. Atrofi, hiperplazi, hipertrofi ve metaplazi, adaptasyon mekanizmalarıdır. Adaptasyon yeteneği aşılırsa, hücre zedelenir. Belirli bir noktaya kadar zedelenme geri dönüşümlüdür. Ama zedeleyici etken şiddetli ve uzun süreli ise geri dönüşümsüz zedelenme ve hücre ölümü gerçekleşir. Adaptasyon, geri dönüşümlü zedelenme ve hücre ölümü, hücrenin normal yapısı ve fonksiyonunda oluşan ilerleyici bozulmanın aşamalarıdır.
ADAPTASYON MEKANİZMALARI
ATROFİ : Hücrede sayısal azalma olmaksızın hücre boyutları ve organel miktarında azalmadır. Organın boyutu küçülür. Organel yıkımı arttığından otofajik vakuoller karakteristiktir.
Fizyolojık: Notokord ve tiroglossal duktus gibi embriyolojik yapıların gerilemesi, doğumdan sonra uterusun involusyonu
Patolojik: İş yükü azalması, innervasyon ve kanlanmasının azalması, beslenme yetersizliği, endokrin uyarı azalması, yaşlanma, basınç gibi nedenler atrofiye yol açar.
HİPERTROFİ : Hücre organelleri ve boyutunda artışla birlikte organda büyümedir. Çoğalma yeteneği olan hücrelerde hiperplazi ile birlikte oluşur. Çoğalamayan hücrelerde ise iş yükü artışı gibi durumlarda tek başına gelişir.
Fizyolojik : Düz kas hücresi nüvelerinde östrojen reseptörü bulunur. Bu nedenle hamilelerde uterusta düz kas hipertrofisi ve hiperplazisi görülür. Hipertrofi baskındır.
Patolojik: Çizgili kas hücreleri çoğalamaz. Bu nedenle hipertansiyonda sol ventrikülde hipertrofi gelişir. Tedavi edilmezse hücrenin adaptasyon yeteneği aşılır ve sol ventrikül dilate olur.
HİPERPLAZİ : Hücrelerde sayısal artış sonucu organın büyümesidir. Çoğalma yeteneği olmayan çizgili kas ve nöronlarda hiperplazi oluşamaz. Çoğalan hücrelerde ise hiperplazi ve hipertrofi genellikle birlikte oluşur.
Fizyolojik :
1. Hormonal hiperplazi: Gebelik ve ergenlikte meme epitelinde hiperplazi ve hipertrofi birlikte oluşursa da, hiperplazi baskındır. Gebe uterusda da hipertrofi ve hiperplazi birliktedir.
2. Kompansatuar hiperplazi: Karaciğerin bir kısmı çıkarılırsa kalan hücreler çoğalarak eski boyuta ulaşmaya çalışır. Unilateral nefrektomi sonrasında, diğer böbrekte kompansatuar hiperplazi oluşur.
Patolojik : Patolojik hiperplazinin en sık nedeni aşırı hormonal uyarıdır.
Endometrial hiperplazi östrojenin artışı veya progesteronla dengelenememesi sonucunda oluşur ve anormal menstrüel kanamanın sık bir nedenidir. Etken ortadan kaldırılırsa hiperplazi geriler. Ancak endometrial hiperplazi karsinom gelişimi için uygun bir zemindir.
Yara iyileşmesinde fibroblast ve kapiller damar hiperplazisi tamir dokusunu oluşturur. Papillomavirüs epidermiste hiperplazi oluşturarak ciltte papillom(verrü) gelişimine yol açar.
METAPLAZİ : Olgun bir hücre tipinin genellikle daha dayanıklı, farklı bir olgun hücre tipine dönüşmesidir. Epitelial hücrelerde daha sıktır ve en sık kolumnar hücrelerin skuamöz hücrelere dönüşümü görülür.
Skuamöz metaplazi :
-Sigara içenlerde ve A vitamini eksikliğinde solunum sisteminde
-Serviks epitelinde inflamasyon ve irritasyona bağlı olarak
-Mesanede taş, kronik inflamasyon, Schistosomiazis
-Tükrük bezi,pankreas ve safra duktuslarında taş varlığı
Metaplazik hücrelerde displazi gelişirse skuamöz (yassı epitel) hücreli karsinom riski artar.
Glandüler metaplazi : En iyi örnek Barrett özefagusudur. Normalde özefagusu döşeyen skuamöz hücreler uzun süreli reflü sonucunda glandüler hücrelere dönüşür. Metaplazik glandüler hücrelerde displazi gelişirse özefagusda adenokarsinom riski artar.
Mezenşimal metaplazi : Nadir görülür. Daha çok lokal zedelenmeye yanıt olarak fibroblastlar kondroblast yada osteoblastlara dönüşerek kıkırdak ve kemik üretirler. Örnek: Myozitis ossifikans
Atrofik organın boyutu küçülür; hipertrofik ve hiperplazik organın boyutu büyür. Metaplazi boyut değişikliği oluşturmaz. Hipoplazi gelişimsel olarak hücrelerin sayısında azalma ve organ boyutunda küçülme ile karakterli olup adaptasyon mekanizması değildir ve atrofi ile karıştırılmamalıdır. Turner sendromu ve Klinefelter sendromundaki hipoplazik gonadlar adaptasyon değil, gelişimsel defektlerdir.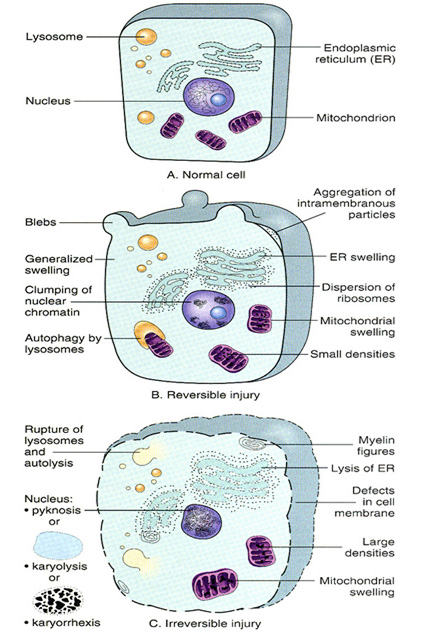
HÜCRE ZEDELENMESİ
Zedelenmeye yol açan nedenler:
Hipoksi: Hücre zedelenmesinin en önemli ve en sık nedenidir. Kardiorespiratuar yetmezlik, anemi, karbonmonoksit zehirlenmesi gibi durumlarda oksijenasyon azalır. İskemi ise arteriel yetmezlik yada venöz drenajın azalması ile oluşur. Oksijenin yanı sıra glikoz gibi metabolitlerin eksikliğide söz konusudur. Anaerobik glikoliz kısa sürer ve bu nedenle iskemide hasar, hipoksiden daha ağır ve hızlı oluşur.
Fiziksel etkenler: Travma, yanık ve donmalar, atmosfer basıncında değişme, radyasyon, elektrik çarpması
Kimyasal madde ve ilaçlar: Hipertonik glikoz ve tuz konsantrasyonları, yüksek oksijen konsantrasyonu, arsenik, civa tuzları ve siyanür gibi toksinler, insektisid ve herbisidler, asbest, CO, alkol, narkotikler ve ilaçlar
Ayrıca enfeksiyöz ajanlar, immünolojik reaksiyonlar, genetik bozukluklar ve beslenme bozuklukları, hücre zedelenmesine yol açabilir.
Zedeleyici etkenler ile ATP yapımı azalır, membran bütünlüğü bozulur, protein sentezi bozulur, hücre iskeleti zedelenir ve DNA hasarı oluşur. Zedelenme önce geri dönüşümlüdür. Zedeleyici etken uzun sürerse yada şiddetli ise, geri dönüşümsüz zedelenme yani hücre ölümü gerçekleşir.
Hipoksik Zedelenme
Hücre hipoksi ile ilk karşılaştığında önce boyutunu ve organel miktarını azaltarak, yani atrofiye giderek daha az oksijenle idare etmeye çalışır. Adaptasyon yeteneği aşıldığında zedelenir. Nöronlar hipoksiye en hassas hücreler olup 3-6 dakikada kaybedilirler. Fibroblast ve iskelet kası hücreleri uzun süre dayanır. Karaciğer ve kalp kası hücreleri 30-40 dakika sonra geri dönüşümsüz olarak zedelenirler.
Hipoksinin hücrede ilk etkilediği organel mitokondri; ultrastrüktürel (elektron mikroskobik) olarak ilk bulgu endoplazmik retikulum şişmesidir.
Hipoksi ile mitokondride ATP yapımı azalır. Enerjiye bağımlı çalışan sodyum pompası bozulur. Sodyum hücre içerisinde birikince dışardan hücre içine su çeker, hücre ve organelleri şişer. Hücre enerji üretebilmek için anaerobik mekanizmaları devreye sokar, laktik asit birikir ve hücre içi Ph düşer. Buna bağlı olarak nükleer kromatin kümelenir. Şişmeye bağlı olarak ribozomlar ER dan ayrılmaya başlar, sitoplazmik membranda köpükler oluşur. Mitokondri hafif derecede şişer ve içerisinde küçük kalsiyum birikintileri oluşur. Hücre iskeleti zedelenir, mikrovillus gibi organeller kaybolur. Lipoprotein disosiasyonu ile myelin figürler oluşur. Glikoz kaybı ve protein sentezinde azalma, hücre fonksiyonunu bozar. Örneğin, koroner tıkanıklıktan 60 saniye sonra kalp kasında kontraksiyon durur ama bu hücre ölümü değildir. Bu aşamada etken ortadan kaldırılırsa hücre kendini tamir eder.
Geri dönüşümsüz zedelenmenin en önemli iki nedeni membranlarda kalıcı hasarın oluşması ve ATP yapımının yeniden başlayamamasıdır. Zedelenen membrandan hücre içine giren kalsiyum mitokodriye yoğun olarak çöker ve ATP yapımını engeller. Zedelenmiş lizozomal membranlardan sızan yıkım enzimlerini (ATPaz, fosfolipazlar, proteazlar, endonükleazlar) aktive ederek otolizi başlatır. Bu nedenle kalsiyum hücre zedelenmesinde önemli bir mediatördür. Geri dönüşümsüz zedelenmede ER erir, otolizle membran fosfolipidleri tam olarak sindirilemediğinden myelin figürlerine dönüşür. Mitokondri ileri derecede şişmiş olup içinde büyük kalsiyum birikintileri görülür. Nüvede kromatin büzüşmesi ile piknoz; kromatinin parçalanması ile karyoreksis ; yada kromatinin tamamen erimesi ile karyoliz görülür. Zamanla tüm hücre myelin figürüne dönüşebilir. Bunlar, diğer hücreler tarafından fagosite edilir yada yağ asidlerine dönüşür. Kalsifikasyon sonucunda, kalsiyum sabunları oluşur.
İntraselüler enzim ve proteinlerin zedelenmiş membrandan sızarak plazmaya geçmesi, hücre ölümünün göstergesidir. Kardiak kreatin kinaz MB ve kontraktil protein olan troponin’in serumda artışı, kalp kasında nekroz gelişiminden 2 saat sonra belirlenebilir.
Hipoksi ile ön planda nekroz oluşursa da, mitokondriden sızan proapoptotik moleküller apoptoza yol açabilir.
ZEDELENME BULGULARI
Geri Dönüşümlü :
• Hücre şişmesi
• ER şişmesi
• Nükleer kromatin kümelenmesi
• Ribozomların ER’dan ayrışması
• Membranda köpük oluşumu ve partiküller
• Mikrovillus kaybı
• Otofaji
• Mitokondride hafif şişme ve küçük partiküller
Geri Dönüşümsüz :
• Membran hasarı ve myelin figürler
• Lizozomal enzimlerin salınımı ve otoliz
• ER erimesi
• Mitokondride belirgin şişme ve büyük dansiteler (Ca++)
• Nüvede piknoz, karyoliz, karyoreksis
Serbest Radikal Hasarı (Oksidatif stres)
Aktif oksijen metabolitleri(serbest radikaller) hücre zedelenmesine yol açar.
Serbest radikallerin oluşmasına yol açan nedenler:
• Radyasyon
• İnflamasyon
• Oksijen toksisitesi
• Kimyasal maddeler (CCI4)
• Reperfüzyon hasarı
• Demir ve bakır gibi metaller
Zedeleme mekanizmaları:
1. Lipid peroksidasyonu ile hücre membranını zedeler (membrandaki E vitamini hasarı azaltır).
2. DNA’da timin ile reaksiyona girerek mutasyona yol açarlar. Hücre yaşlanması ve maliğn tümör gelişimine yol açabilir (karsinogenez).
3. Polipeptid parçalanması veya proteinlerin çapraz bağlanması ile enzim aktivitesinde kayıp oluşur.
İyonize radyasyonun hücreyi zedeleme etkisi maliğn tümör tedavisinde kullanılmakla birlikte karsinogenez etkisi nedeni ile lösemi gibi sekonder tümörlerede yol açabilir.
Akut inflamasyonda fagositik hücrelerin bakteriyi öldürmek için ürettikleri serbest radikaller hücre dışına sızarak çevre dokuyu zedeleyebilir. Nitrik oksid serbest radikaldir.
Yüksek basınçlı oksijen tedavisi yenidoğanda retrolental fibroplaziye yolaçabilir.
Karbon tetraklorür kuru temizlemede kullanılan bir toksindir. Karaciğerde metabolize olduktan sonra bir serbest radikal olan karbon triklorüre dönüşür. Karaciğerde apoprotein sentezini bozarak yağlanma ve ağır durumlarda mitokondri hasarı ile nekroza yol açar.
Reperfüzyon hasarı ise iskemik bir bölgeye , hücre ölümü gerçekleştikten sonra, dolaşımın yeniden sağlanması ile oluşur. Dolaşımla gelen nötrofillerden açığa çıkan serbest radikaller, sitokinler, inflamatuar mediatörler ve kalsiyum hasarı daha da arttırır. Antioksidanlar ve antiinflamatuar ilaçlar faydalı olabilir. Ayrıca nekrotik dokuda IgM birikimi olduğu ve dolaşımla gelen komplemanı aktive ederek hasarı ağırlaştırabileceği ileri sürülmektedir.
Demir ve bakır, intraselüler reaksiyonlar sırasında, serbest elektron alıp-vererek serbest radikal oluşumunu katalizler.
Antioksidanlar
• Süperoksid dismutaz
• Glutatyon peroksidaz
• Katalaz
• Vit. E, A, C
• Sistein, Glutatyon
• Serüloplazmin, Transferrin, Albumin
Kimyasal Zedelenme
Direkt etkili zedeleyiciler:
Vücuda alındığı yapıda zedelenme oluşturan kimyasal etkenlerdir.
Merkürik klorid hücre membranını direkt zedeler, transportu bozar, permeabilite artar. En çok GİS ve böbrek etkilenir. Siyanür sitokrom oksidazı etkileyerek oksidati fosforilasyonu bloke eder.
Antineoplastik – antibiotikler direkt sitotoksik etki yapar.
İndirekt etkili zedeleyiciler: Vücuda alındığı şekilde değil;dönüştüğü metaboliti ile zedelenme oluşturan kimyasal etkenlerdir.
CCI4 kuru temizlemede kullanılır. p450 enzim sisteminde CCI3 ‘e dönüşerek serbest radikal etkisi yapar. Asetaminofen de indirekt etkilidir.
MORFOLOJİ
GERİ DÖNÜŞÜMLÜ ZEDELENME
Hücre Şişmesi : Bulanık şişme
Mikroskobik : Hidropik değişiklik, vakuoler dejenerasyon (ER şimesine bağlı)
Makroskobik : Organda solukluk, turgor artışı, ağırlık artışı
Yağlı Değişiklik : Özellikle hepatosit ve myokard hücrelerinde sık.. İskemik, toksik, metabolik hasara bağlı
Mikroskobik : Sitoplazmada küçük lipid vakuolleri ile mikroveziküler, büyük tek bir vakuol ile makroveziküler yağlanma
Makroskobik : Organ büyük, sarı renkte, parlak ve kaygan
GERİ DÖNÜŞÜMSÜZ ZEDELENME
Hücre ölümü iki şekilde oluşur: Nekroz ve apoptoz
Nekroz : Yaşayan bir dokuda hücre ölümünü izleyerek oluşan morfolojik değişikliklerdir. Işık mikroskobunda 4-12 saat içinde görülebilir hale gelir. Farklı nekroz tipleri görülür. Eğer hücre kendi lizozomal enzimleri ile (otoliz), yada ortamdaki lökositlerin enzimleri ile sindirilirse likefaksiyon nekrozu gelişir ve hücre tamamen ortadan kalkar (enzimatik sindirim). Hücre içi pH çok düşerse, tüm proteinler gibi lizozomal enzimlerde denatüre olur ve otoliz durur. Bu durumda hücre tamamen ortadan kalkmaz ve mikroskobik incelemede hücre hayalleri görülebilir; koagulasyon nekrozu oluşur (protein denatürasyonu). Nekrotik hücrelerin içeriği membrandan sızdığı için inflamatuar yanıta yol açar.
Nekrotik hücrelerde, sitoplazmada bazofili gösteren RNA kaybı ve denatüre proteinlerin eozin bağlaması sonucunda eozinofili artar. Glikojen partiküllerinin kaybı ile homojen görünüm oluşur. Enzimler organelleri sindirdiği için, sitoplazma vakollü görünümdedir. Hücreler sonuçta myelin figürlerine dönüşür. Fagositoz yada kalsifikasyonla sonuçlanır.
Koagulasyon nekrozu : Beyin hariç tüm dokularda hipoksiye bağlı oluşan nekrozdur. Myokard enfarktüsü en iyi örnektir. Hızla büyüyen maliğn tümörlerde de beslenme bozukluğuna bağlı olarak oluşabilir.
Likefaksiyon nekrozu : Beyinde hipoksi – iskemi; tüm vücutta fokal bakteriel ve nadiren mantar enfeksiyonlarında heterolize bağlı olarak oluşur. Apse odakları örnek verilebilir. Sıvı, visköz kitle oluşur.
Gangrenöz nekroz:Ayrı bir nekroz tipi değildir. Özellikle alt ekstremitede dolaşım bozukluğu ile oluşan koagulasyon nekrozu odağına bakteriel enfeksiyonun, dolayısı ile likefaksiyon nekrozunun eklenmesi ile oluşur (Yaş gangren).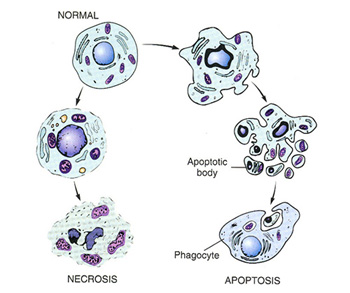
Kazeifikasyon nekrozu: Koagulasyon nekrozunun farklı bir şeklidir. En sık tüberküloz enfeksiyou;daha nadiren derin mantar enfeksiyonlarında görülür. Nekroz odağı granülomatöz inflamasyon ile çevrili amorf granüler debris olarak görülür.
Yağ nekrozu : Pankreas dokusu ve peritoneal kaviteye aktive olmuş lipazın sızması ile oluşan fokal yağ dokusu zedelenmesidir. Yağ asitleri kalsiyumla birleşerek beyaz renkli odaklar oluşturur; kalsiyum sabunları denir. Nekrotik yağ hücreleri, bazofilik kalsiyum birikimleri ve çevresinde iltihabi hücreler görülür.
Ayrıca memede travmatik yağ nekrozu görülebilir.İmmünolojik olaylarda, özellikle Tip III aşırı duyarlılık reaksiyonunda, damar duvarında oluşan zedelenme fibrinoid nekrozdur.
Apoptoz : Hücre ölümünün diğer morfolojik biçimidir. Programlı hücre ölümüde denir. Nekroz her zaman patolojik iken, apoptoz fizyolojik ve patolojik olarak oluşabilir.
Fizyolojik:
• Embriyogenesisi sırasında gereksiz bölgelerin ortadan kaldırılması
• Erişkinde hormon bağımlı involusyon: menstrüel sikluda endometrial dökülme, menapozda ovarian foliküler atrezi, laktasyon bitince memede küçülme, kastrasyon sonrası prostatik atrofi
• Kript epiteli gibi sürekli çoğalan hücrelerde, belirli bir sayının korunabilmesi için, hücre delesyonu
• İnflamasyon ve immün reaksiyonlarda, görevi biten hücrelerin ortadan kaldırılması
• Self-reaktif lenfositlerin eliminasyonu
• Viral enfeksiyonlar, tümörler ve transplant rejeksiyonunda sitotoksik T lenfositlerinin hücreleri öldürmesi
Patolojik:
• Zedeleyici etkenlere bağlı oluşan hücre ölümü: radyasyon, kanser ilaçları ile oluşan DNA hasarı, hafif dereceli hipoksi, endoplazmik retikulumda dejenere proteinlerin birikimi ile oluşan stres
• Viral hepatit gibi viral enfeksiyonlarda, enfekte hücrelerin ölümü (Councilman cisimciği)
• Duktus tıkanıklığı sonrasında, pankreas, parotis ve böbrekde parankimal atrofi
• Tümörlerde hücre ölümü
• Mitokondrial permeabilite bozukluğu ile, nekrotik olaylarda apoptozunda eklenmesi
• Liken plan gibi bazı cilt hastalıklarında görülen Civatte cisimciği
Morfoloji
• Hücre büzüşmesi: Hücre küçülür, sitoplazma yoğunlaşır, organeller sıkışır.
• Kromatin kondansasyonu: en karakteristik bulgudur. Kromatin, nükleer membran altında birikir. Nüve birkaç parçaya ayrılabilir.
• Sitoplazmik kabarcık ve parçalar, apoptotik cisimcikleri oluşturur.
• Apoptotik hücre yada cisimcikler, makrofajlar tarafından fagosite edilerek sindirilir.
• Mikroskobik incelemede yuvarlak yada oval, yoğun eozinofilik sitoplazmalı, koyu nükleer fragmanlar içeren, tek yada küçük gruplar halinde, apoptotik hücreler görülür.
• İnflamatuar yanıt oluşturmaz.
Biyokimyasal Bulgular
• Protein yıkımı: Kaspazların oluşturduğu protein hidrolizi ile nüve ve hücre iskeleti zedelenir. Kaspazlar, DNAzları aktive ederek DNA fragmantasyonuna yol açar.
• DNA yıkımı: Endonükleaz aktivitesi, DNAzlar
• Fagositik tanınma: Apoptotik hücre membranlarında fosfotidilserin ve trombospondin ekspresyonu, opsonizasyona yol açar ve fagositoz ile sonuçlanır.
Mekanizma
• Ekstrensek yol: Hücre yüzeyindeki ölüm resptörleri TNF reseptör ailesindendir. En iyi bilinen TNFR1 ve ilişkili olduğu Fas proteinidir. Fas ligand (FasL) ile birleşince kaspazlar aktive olur ve apoptoz devreye girer.
• İntrensek (mitokondrial) yol: Mitokondrial permeabilite artışı ve proapoptotik moleküllerin sitoplazmaya salınımı ile olur. Büyüme faktörleri ve diğer sağkalım sinyalleri anti-apoptotik Bcl-2 protein ailesini uyarır. En önemli anti-apoptotik proteinler Bcl-2 veBcl-x dir. Bcl-2, foliküler lenfomada rol alan onkogendir. Sağkalım sinyalleri kaybolursa, bu iki protein yerini Bak, Bax ve Bim gibi pro-apoptotik olanlara bırakır ve mitokondrial permeabilite artar. Sitokrom oksidaz gibi enzimler salınarak kaspazları uyarır.
Örnekler:
• Büyüme faktörü azalması: hormonların azalması, antijen ve sitokin uyarısı kaybolan lenfoaitler, sinir büyüme faktörü ile uyarılmayan nöronlar…İntrensek mekanizma devreye girer.
• DNA hasarı: Apoptozun fizyolojik olarak maliğn tümör gelişiminden koruyucu etkisi vardır. Bir hücrede mutasyon geliştiğinde önce DNA tamir mekanizmaları devreye girer. Bu mekanizma başarılı olamazsa p53 geni devreye girerek Bax’ı uyarır, apoptozu başlatır ve mutant hücre öldürülerek ortadan kaldırılır. Apoptoz gerçekleşemezse mutant hücre çoğalmaya devam eder ve maliğnite riski artar.
• TNF reseptör ailesi: Self reaktif lenfositlerin apoptozu ve otoimmün hastalıkların engellenmesi bu şekilde olur. TNF apoptoza yol açabilir.
• Sitotoksik T lenfositleri: Enfekte hücreler üzerindeki yabancı antijenleri tanıyarak perforin salgılar. Hücre yüzeyinde delik açılır ve granüllerindeki granzim B (serin proteaz) hücreye girerek kaspazları aktive eder. Ayrıca sitotoksik T lenfositlerinin yüzeyinde FasL bulunur ve apoptoza yol açar.
Apoptoz Disregülasyonu:
Apoptoz defekti:
• Kanserler; özellikle p53 mutasyonu ile oluşanlar, hormona bağlı gelişenler (meme, over, prostat) ve foliküler lenfoma (Bcl-2 mutasyonu)
• Otoimmün hastalıklar
Apoptoz artışı:
• Spinal muskuler atrofi gibi , bazı nöronların kaybı ile giden nörodejeneratif hastalıklar
• MI ve serebral enfarktüs gibi iskemik hastalıklar
• Viral enfeksiyonlarda, enfekte hücrelerin ölümü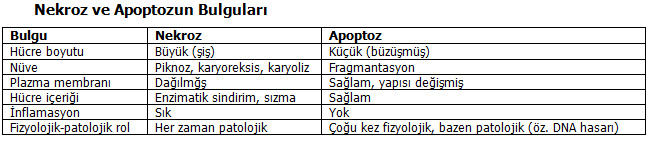
Subselüler Zedelenme
Zedeleyici etkilere bağlı olarak hücre organellerinde oluşan değişikliklerdir.
Hücre İskelet Anomalileri :
• Chediak-Higashi sendromu mikrotübül polimerizasyon defektidir. Lizozomla fagozom birleşemez ve fagositoz bozulur. Lökositlerin sitoplazmasında büyük, anormal lizozomlar oluşur.
• İmmotil silia sendromu (Kartagener sendromu) ise mikrotübül organizasyon defektidir. Spermin motilitesi bozulduğundan erkekte sterilite , siliaların hareketi bozulduğundan alt solunum yolu enfeksiyonları sonrasında bronşiektazi gelişir.
• Sitozalasin B ve Amanita falloidesin toksini olan falloidin, hücre iskelet elemanleından aktin filamanlarını bağlar. Lökosit harakatlari ve fagositoz bozulur.
• Alkolik hepatit ve diğer bazı karaciğer hastalıklarında görülen Mallory cisimciği intermedier flaman keratin birikimidir. Alzheimer hastalığında görülen nörofibriler yumaklar ise mikrotübül ile ilişkili proteinler ve nöroflamandan oluşur.
• Hücre iskelet proteinleri, yüzey reseptörleri ile ilişkilidir. Wiskott-Aldrich sendromu, lenfosit antijen reseptörlerini hücre iskeletine beğlayan proteinlerde defekt ile karakterli herediter hastalıkltır. Ekzema, trombosit anomalileri ve immün yetmezlik görülür.
Mitokondrial Değişiklikler
• Beslenme bozukluğu ve alkolik hepatitde ileri derecede büyümüş mitokondriler (megamitokondri) görülebilir.
• İskelet kasının bazı kalıtımsal metabolik hastalıklarında (mitokondrial myopati) anormal krista içeren büyük mitokondriler görülebilir.
• Böbrek, tiroid, paratorid ve tükrük bezlerinde büyümüş ve çoğalmış mitokondri içeren, geniş eozinofilik sitoplazmalı hücrelerden oluşan tümörlere onkositom denir. Hücrelere de onkositik hücre denir. Hurtle hücreleri bu grupta yer alır.
DER İndüksiyonu:
• Barbitüratlar düz endoplazmik retikulum ve p450 enzimlerinin sentezini arttırır. Tolerans artar, adaptasyon gelişir. Steroid, alkol, aril hidrokarbonlar, insektisidler gibi maddelerin metabolizması hızlanır.
Hücre İçi Birikimler
Yağlı Değişiklik ( Steatoz)
Birikimler trigliserid, kolesterol ve kolesterol esterleri yapısında olabilir.
Karaciğer, kalp kası, iskelet kası ile böbrek tübül hücrelerinde trigliserid birikir.
Karaciğerde:
• Hepatotoksinler ,örneğin alkol, mitokondri ve DER fonksiyonunu bozar.
• CCI4 ve protein malnütrisyonu apoprotein sentezini azaltır.
• Anoksi yağ asidi oksidasyonunu bozar.
• Açlık ve Diabetes Mellitus periferik depolardan yağ asiti mobilizasyonunu arttırır,karaciğere giren yağ asiti artar.
• Alkol ve orotik asit karaciğerden lipoprotein salınımını azaltır.
Kalpte :
• Uzamış orta dereceli hipoksi ile bant tarzında sarı renkte yağ birikimi kaplan görünümünü oluşturur.
• Belirgin hipoksi ve difteri gibi ağır myokarditlerde ise diffüz yağlanma oluşur.
Kolesterol ve kolesterol esterleri
• İnfalmatuar ve nekrotik alanlar çevresinde köpüklü histiositler
• Aterosklerotik plaklarda köpüklü düz kas hücreleri ve makrofajlar
• Kantomlarda köpüklü makrofajlar içerisinde kolesterol ve kolesterol esterleri
• Kronik kolesistitte lmina propria içerisinde kolesterolle yüklü makrofajlar: kolesterolozis
Proteinler
Hücre içi protein birikimleri yuvarlak, eozinofilik damlacıklar olarak görülür.
• Bazı hastalıklarda, protein birikiminin sebebi yapısındaki bozukluktur. Ribozomlarda yapılan polipeptid zincirleri alfa heliksleri yada beta kümeleri olarak düzenlenir (protein kıvrılması). Protein fonksiyonu ve organellere transportu için bu düzenleme gereklidir. Kıvrımlar düzgün değilse, normal koşullarda şaperonlar, proteinleri düzeltir. Bazı şaperonlar ısı gibi strese bağlı oluşur (ısı-şok proteinleri, hsp70, hsp90 gibi) ve proteinleri korurlar. Proteinler tamir edilemezse, yine bir ısı-şok proteini olan ubiquitin ile proteazom kompleksine taşınarak parçalanırlar. Parçalanmayan anormal yapıdaki proteinler hücre içerisinde birikir.
- Defektif intraselüler transpot ve sekresyon: Alfa-1 antitripsin yetmezliği’nde, kısmen kıvrılmış defektif protein, karaciğerde, ER’da birikir ve hücre dışına salınamaz. Dolaşımda enzimin düşük olması amfizeme yol açar. Kistik fibrozis’de klorid kanal proteini şaperondan ayrılamaz ve fonksiyonu bozulur. Familial hiperkolesterolemi’de ise LDL reseptör proteininde defekt vardır.
- Kıvrılmamış yada yanlış kıvrılmış protein birikimi ile oluşan ER stresi: Bu durumda hücrede şaperon artışı ve protein translasyonunda azalma oluşur. Kaspazlar aktiflenerek apoptoz uyarılır. Genetik mutasyon, yaşlanma yada bilinmeyen nedenlerle anormal proteinlerin birikmesi Alzheimer, Huntington ve Parkinson hastalıkları gibi nörodejeneratif hastalıklar ve tip II DM da suçlanmaktadır.
- Anormal protein birikimi: Anormal kıvrımlı proteinlerin birikimi, hücre fonksiyonunu bozabilir. Birikimler hücre içi yada dışında olabilir. Bazı amiloidoz tipleri bu grupta yer alır (proteinopatiler).
• Nefrotik sendromda filtrata geçen proteinlerin bir kısmı proksimal tübülde geri emilir ve proksimal tübül epitel hücreleri lizozomları içinde birikir. Geri dönüşümlüdür.
• Plazma hücresi sitoplazmasında, granüllü endoplazmik retikulum içinde Ig birikimi Russel cisimciği; plazma hücresi nüvesi içerisinde Ig birikimi ise Dutcher cisimciği olarak isimlendirilir.Multiple myelom ve bazı lenfoma tiplerinde belirgindir.
Glikojen
Glikoz yada glikojen metabolizma bozukluklarında (ör: DM, glikojen depo hastalıkları) glikojen hücre içinde birikir ve berrak vakuol olarak görülür.
• Diabetli hastalarda üriner filtrata çıkan glkozun bir kısmı proksimal tübülde geri emilir ve tübül epitel hücresi içerisinde berrak vakuol olarak görülür. Buna Armanni-Ebstein bulgusu denir.
Hematoksilen-Eozin ile boyalı kesitlerde protein birikimi pembe rekte; yağ,glikojen ve su birikimi berrak vakuol olarak görülür. Berrak vakuol PAS ile boyanırsa glikojen; oil red-o,Sudan black gibi yağ boyaları ile boyanırsa yağ; bunlardan biri ile boyanmıyorsa biriken madde sudur.
Pigmentler
• Egzojen : Karbon-kömür tozu ve dövme pigmenti
En sık egzojen pigment olan karbon yada kömür tozu inhale edildiğinde alveoler makrofajlar tarafından fagosite edilir, lenfatikler aracılığı ile trakeobronşial lenf düğümlerine taşınır. Birikimi akciğer ve lenf düğümlerinde siyahlaşmaya yol açar ve antrakoz denir. Kömür madeni işçilerinde yoğun birikim pnömokonyoza yol açabilir.
Dövme pigmenti ise dermal makrofajlar tarafından fagosite edilir ve sindirilemediğinden ömür boyu lokalize olarak kalır. İnflamatuar yanıt uyandırmaz.
• Endojen : Lipofusin, melanin, hemoglobin türevleri
Lipofusin (lipokrom-yaşlanma) pigmenti uzun ömürlü hücreler ve atrofik hücrelerde organel yıkımı sonucunda, organel membranlarındaki poliansatüre lipidlerin peroksidasyonu ile oluşur.Tam olarak sindirilemediğinden lizozomlar içinde birikir ve sarı-kahverengi, granüler pigment olarak görülür. Hücrede zedelenme oluşturmaz, çok fazla miktarda birikirse organda kahverenkte görünüm oluşturur. Serbest radikal hasarı ve buna bağlı oluşan lipid peroksidasyonunun göstergesidir. Yaşlılarda kalp , karaciğer ve nöronlarda belirgindir. Yaşlı hastaların kalbinde görülebilen kahverengi atrofi gibi...Ağır malnütrisyonlu ve kaşektiklerde de belirgindir.
Melanin,tirozinaz enzimi aktivitesi ile melanositler tarafından üretilen endojen pigmenttir. Tirozinaz enziminin, tirozini okside ederek dihidroksifenil alanine dönüştürmesi ile oluşur. Melanositler epidermisin bazal tabakasında bulunan nöroektoderm kökenli hücrelerdir. Tirozinaz enzimi eksikliğinde Albinizm ; lokalize melanosit kaybı ile Vitiligo oluşur.
Alkaptonüri nadir bir metabolik hastalıktır. Cilt,bağ dokusu ve kıkırdakta siyah-kahverenkte homogentisik asit birikir; okronozis denir.
Hemosiderin hemoglobin türevi, altınsarısı-kahverenkte bir pigmenttir ve normal koşullarda kemik iliği, dalak ve karaciğerdeki mononükleer fagositik hücrelerde az oranda bulunabilir. Lokalize yada sistemik demir artışı ferritin yapısında hemosiderin birikimine yol açar. Lokalize artışı hematom çevresindeki makrofajlar içerisinde görülür. Önce hemoglobine bağlı kırmızı-mavi renk; zamanla biliverdine bağlı sarı-yaşil görünüm; daha sonra bilirübin ve en sonunda hemosiderine bağlı sarı-kahve renk oluşur. Sistemik demir artışında ise hemosiderin pek çok organ ve dokuda birikerek Hemosiderozise yol açar. Hemosiderozis hücre ve organın fonksiyonunu bozmaz ve patolojik tablo oluşturmaz. Ama aşırı derecede demir artışı ile karakterli Hemokromatozis de karaciğer ve pankreasda fibrozis sonucu siroz, diabetes mellitus, kalp yetmezliği gibi tablolar oluşur.
Bilirubin hemoglobin türevi olmakla birlikte demir içermeyen safra pigmentidir. Hücre ve dokularda birikimi sarılık oluşturur. Tüm dokularda biriksede en fazla birikim karaciğer ve böbrektedir.Mikroskopik olarak yeşil-kahve-siyah renkte, mukoid, amorf, globuler birikim olarak görülür.
Patolojik Kalsifikasyon
• Distrofik kalsifikasyon : Nekrotik odaklar, aterom plakları, zedelenmiş kalp kapacıklarına kalsiyum çökmesidir. Kalsiyum metabolizması ve serum düzeyi normaldir. Papiller tiroid karsinomu, overin seröz papiller karsinomu ve menenjiomda görülen psammom cisimcikleride distrofik lameller kalsifikasyondur. Tüberkülozda görülebilir.
• Metastatik kalsifikasyon : Kalsiyum metabolizmasında değişiklik ve serum düzeyinde artış vardır.Hiperparatiroidizm, multiple myelom, lösemi, kemiğe metastaz gibi kemik yıkımı artışı, vitamin D intoksikasyonu, süt-alkali sendromu, sarkoidoz, paraneoplastik sendromlar (ör: akciğerin skuamöz hücreli karsinomu) gibi hiperkalsemik durumlarda görülebilir.Tüm vücutta oluşabilirsede en sık kan damarları, böbrek, akciğer ve mide mukozasının intersisyel bölgelerinde birikir. Çoğu kez klinik bulgu oluşturmaz. Ağır durumlarda akciğerde solunum bozuklukları ve böbreklerde nefrokalsinozise bağlı hasar oluşturur.
HÜCRE ÇOĞALMASI
Zedelenen bir doku iki şekilde iyileşir:
1. Rejenerasyon
2. Skar dokusu oluşumu
Bağ dokusu çatısı sağlam ve hücrenin çoğalma yeteneği varsa rejenerasyon ; bağ dokusu çatısı yıkılmış veya hücrenin çoğalma yeteneği yoksa skar dokusu oluşumu gerçekleşir.
Yalnız epidermisin zedelendiği yüzeyel yaralanmalarda tam rejenerasyon olurken; dermiside içine alan insizyonel ve eksizyonel yaralanmalar skar ile iyileşir.Myokard enfarktüsü, kalp kası hücreleri çoğalamadığı için, skar ile iyileşir.Perikard, plevra ve peritonun inflamasyonları skar ile iyileşirken, parietal ve visseral yapraklar arasında adezyon oluşur ve konstriktif perikardit gibi komplikasyonlar gelişebilir. Parankimal organlarda, inflamatuar dokunun granülasyon dokusu ve sonunda fibrozise dönüşmesi, organizasyon olarak isimlendirilir.
Karaciğerde karbon tetraklorür gibi toksik bir madde, tek seferde ve yüksek bir dozda alınırsa, hepatositlerin %50’den fazlası ölür ama bağ dokusu çatısı zedelenmez. Hasta yaşarsa rejenerasyon gerçekleşir. Toksin küçük dozlarda, uzun süre alınırsa ekstraselüler matriks zedelenir ve fibrozis gelişir.
Sürekli çoğalan (labil) hücreler: Cilt, oral kavite, vajen, serviks gibi skuamöz epitelle döşeli bölgeler; tükrük bezi, pankreas gibi glandüler organların salgı duktus epiteli, gastrointestinal sistem ve uetrusun kolumnar epiteli, üriner tarktüsün transisyonel epiteli, kemik iliği ve diğer hematopoetik doku hücreleri…. Sınırsız çoğalma yeteneği olan kök hücreler olgun hücreleri oluşturur.
Sessiz (stabil) hücreler: Karaciğer, böbrek, pankreas gibi tüm glandüler epitel hücreleri, fibroblast, düz kas ve endotel hücresi gibi mezenşimal hücreler, istirahat halindeki lenfosit ve diğer lökositler... Bu hücreler G0 fazında iken, uyarı ile G1’e geçerler.
Bölünmeyen (kalıcı) hücreler: Nöronlar, kalp kası ve iskelet kası hücreleri... Çoğalma yetenekleri yoktur. Son çalışmalar erişkin beyninde kök hücrelerden nöronogenezis oluştuğunu göstermiştir. Çizgili kas hücreleri bölünmediği halde, endomisyal kılıfa tutunan satellit hücrelerin rejeneratif kapasitesi olduğu gösterilmiştir. Yaralanan kas lifleri ucuca getirildiğinde rejenerasyon gerçekleşebilirse de bu pratikte pek mümkün değildir.
Erişkinde hemopoetik kök hücrelerinin mezodermal, ektodermal ve endodermal diferansiasyon gösterebildiği ortaya çıkarılmış: Multipotent erişkin progenitör hücreleri…Kas, beyin ve cilttede benzer hücreler bulunmuş. Karaciğerde, bilier duktuler sistem ve hepatositler arasındaki Hering kanallarında, oval hücreler denilen, karaciğer ve safra yolu epiteline dönüşebilen kök hücreler belirlenmiş. Bunların fonksiyonları halen araştırılmaktadır.
Hücre çoğalmasında polipeptid yapıdaki büyüme faktörleri hücre yüzeyindeki reseptörlere bağlanıp uyarırlar. Bu reseptörler aracılığı ile tirozin kinaz aktive olur. Sitoplazmada sinyal taşıyıcı maddeler fosforilize edilir ve ras proteinleri, fosfolipaz C- g ve Raf-1 gibi ikincil mesaj taşıyıcılar ortaya çıkar. Çoğalma sinyalleri kinazlar aracılığı ile nukleusa taşınır. Transkripsiyon başlar, DNA sentezi ve arkasından hücre bölünmesi gerçekleşir. Hücrenin bölünme aşaması siklin proteinleri ile yönetilir. Siklinler kinazlarla bileşip mitozda rolü olan substratları fosforilize ederler.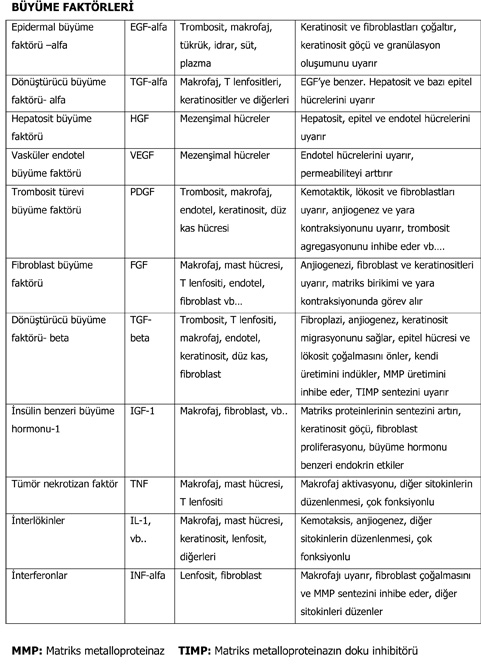
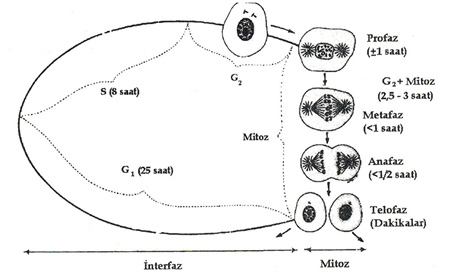
HÜCRE SİKLUSU
1) İnterfaz
2) Mitoz: Hücre bölünmesinin görülebilen kısmı.
İnterfazda görülebilen morfolojik değişiklik yoktur. G1 fazında bir önceki siklusde oluşan küçük yavru hücre normal boyutuna çıkar. RNA ve protein sentezi yapılır (25 saat). S fazında DNA sentezlenir (8 saat). G2 fazında mitozda kullanılacak enerji üretilir, mikrotübüller sentezlenir. G2 vemitoz birlikte 2.5-3 saat sürer.
Mitoz ise profaz, metafaz, anafaz ve telofazdan oluşur.
Profaz : Nükleer kromatin kıvrımlaşır; nüve zarfı sağlamdır.
Metafaz : Nükleer zarf ve nüve kaybolur; kromozomlar ayrışır ve dağılır; mikrotübüllere tutunur.
Anafaz : Oluşan kardeş kromatidler karşı kutuplara ilerler.
Telofaz : Oluşan yeni hücrelerin nüveleri görünür hale gelir; kromozomlar yarı ayrışmış halini korur. Nükleol, kromatin ve nükleer zarf yeniden oluşur. Sindirim sistemi ve epidermiste hücre çoğalması sık; pankreas ve tiroidde yavaştır.

